Jako teplo, má i elektřina, jenže v jiné formě, jistou všudy přítomnost. Téměř žádná změna na zemi nemůže proběhnout, aniž se přitom dají prokázat elektrické jevy. Odpařuje-li se voda, hoří-li plamen, dotýkají-li se dva různé nebo různě zahřáté kovy nebo železo a roztok modré skalice atd., probíhají přitom kromě nápadnějších fysikálních a chemických jevů současně také elektrické procesy. Čím přesněji zkoumáme nejrůznější přírodní pochody, tím více narážíme na stopy elektřiny. Přes tuto svou všudypřítomnost, přes fakt, že je elektřina po půl století stále více vtahována do průmyslových služeb člověka, je právě tou formou pohybu, o jejíž podstatě stále ještě panuje největší nejasnost. Objev galvanického proudu je asi o 25 let mladší než objev kyslíku a znamená pro učení o elektřině nejméně tolik, co objev kyslíku pro chemii. A přece, jaký je ještě dnes rozdíl mezi oběma obory! V chemii, zejména dík Daltonovu objevu atomových vah, vládne pořádek, relativní jistota toho, čeho bylo dosaženo, a soustavný, skoro plánovitý útok na dosud nedobyté území, který lze srovnat s pravidelným obléháním pevnosti. V nauce o elektřině chaotický balast starých, nejistých, ani definitivně nedokázaných, ani definitivně nevyvrácených pokusů; neurčitá tápání v temnotě, vzájemně nesouvisící zkoumání a experimentování mnoha isolovaných jednotlivců, kteří útočí na neznámé území roztříštěně, jako horda kočovných nájezdníků. Ovšem, takový objev, jako byl Daltonův, který dal centrum celé vědě a pevnou basi jejímu zkoumání, takový objev musí být na poli nauky o elektřině teprve učiněn. Je to hlavně tento neurovnaný stav nauky o elektřině, znemožňující zatím vytvoření obsáhlé theorie, který způsobuje, že na tomto poli jednostranně převládá empirie, ta empirie, která si pokud možno sama zakazuje myšlení a která právě proto nejenom nesprávně myslí, ale není ani schopna pozorovat správně skutečnosti, nebo je alespoň správně popsat, která se tedy zvrací v protiklad skutečné empirie.
Má-li být vůbec pánům přírodovědcům, kteří nevědí, co špatného už by řekli o nesmyslných aprioristických spekulacích německé přírodní filosofie, doporučena četba theoreticko-fysikálních spisů empirické školy, pak to platí zejména o nauce o elektřině. Vezměme spis z roku 1840: „An Outline of the Sciences of Heat and Electricity” by Thomas Thomson.[2] Starý Thomson byl svého času autoritou; přitom měl již k disposici velmi významnou část prací dosud největšího badatele v oboru elektřiny, Faradaye. A přece obsahuje jeho kniha při nejmenším stejně nesmyslné věci jako mnohem starší hegelovská přírodní filosofie. Na př. popis elektrické jiskry by mohl být přeložen přímo z příslušné stránky Hegela. Oba vypočítávají všechny ty divy, které byly zdánlivě v jiskře objeveny před poznáním její skutečné podstaty a mnohonásobné rozmanitosti a které se teď ukázaly většinou jako speciální případy nebo omyly. Nejenom to. Thomson vypravuje na str. 446 docela vážně hrůzostrašné historky Dessaignesovy, že prý se při stoupání barometru a klesání teploměru sklo, pryskyřice, hedvábí atd. nabíjejí při ponoření do rtuti negativní elektřinou, při klesání barometru a stoupání teploty kladnou elektřinou; že se zlato a některé jiné kovy v létě ohřátím nabíjejí positivně, ochlazením negativně, a v zimě naopak; že jsou při vysokém tlaku a severním větru silně elektrické, kladně při stoupání, záporně při klesání teploty atd. Tolik pro posouzení věcné stránky. Pokud jde o aprioristickou spekulaci, dává Thomson k lepšímu následující konstrukci elektrické jiskry, která nepochází od nikoho menšího, než je sám Faraday. „Jiskra je výboj neboli zeslabení polarisovaného indukčního stavu mnoha dielektrických částeček pomocí zvláštního působení několika málo těchto částeček, které zaujímají velmi malý a omezený prostor. Faraday předpokládá, že ony nečetné částečky, na nichž probíhá výboj, se nejen navzájem odsunují, nýbrž dočasně nabývají zvláštního, vysoce aktivního (highly exalted) stavu; to znamená, že všechny je obklopující síly jsou vrženy jedna po druhé na ně, čímž jsou částice uvedeny v příslušnou intensitu stavu, která snad odpovídá intensitě při chemickém slučování atomů; že pak ony síly vybíjejí ― podobně jako atomy vybíjejí své síly ― nám dosud neznámým způsobem, a to je konec všeho (and so the end of the whole). Konečný účinek je přesně takový, jako by na místo vybíjejících se částic přišla kovová částice, a nezdá se nemožným, že ,se oba akční principy jednou ukáží totožnými.”[3] „Uvedl jsem,” dodává Thomson, „toto Faradayovo prohlášení jeho vlastními slovy, protože mu dobře nerozumím.” To se přihodí jistě také jiným lidem, podobně jako když u Hegela čtou, že v elektrické jiskře „nevstupuje zvláštní materiálnost nabitého tělesa ještě do procesu, nýbrž je v něm určena jen elementárně a jako projev duše”, a že elektřina je „vlastní hněv, vlastní vzbouření tělesa”, jeho „hněvivé samo”, které „vystupuje na každém tělese, je-li podrážděno” („Naturphilosophie”, § 324, dodatek)[4]. A přece je základní myšlenka u obou, u Hegela i Faradaye stejná. Oba se brání představě, že by elektřina nebyla stav hmoty, nýbrž nějaká zvláštní hmota. A poněvadž v jiskře vystupuje elektřina zdánlivě samostatně, volná a oddělena ode všech cizích materiálních substrátů, a přece smyslově vnímatelná, došli oba za tehdejšího stavu vědy nutně k myšlence, že jiskra je pomíjející forma projevu nějaké „síly”, na okamžik osvobozené ode vší hmoty. Pro nás je hádanka ovšem rozřešena od té doby, kdy víme, že mezi kovovými elektrodami při výboji skutečně přeskakují „kovové částice”, a tedy že „zvláštní materiálnost nabitého tělesa” skutečně „vstupuje do procesu”.
Jako teplo a světlo byly, jak známo, původně také elektřina a magnetismus chápány jako zvláštní nevažitelné substance. U elektřiny se došlo brzy k představě dvou protichůdných substancí, dvou „fluid”, jednoho positivního a jednoho negativního, které se v normálním stavu neutralisují, dokud od sebe nejsou odděleny lak zvanou „elektrickou rozlučovací silou”. Můžeme pak nabít dvě tělesa, jedno positivní, jedno negativní elektřinou. Spojíme-li obě třetím, vodivým tělesem, dojde k vyrovnání, podle okolností buď naráz, nebo trvalým proudem. Náhlé vyrovnání se zdálo jednoduchým a pochopitelným, ale vysvětlení proudu působilo potíže. Proti nejjednodušší hypothese, že se v proudu pohybuje jen kladná nebo jen záporná elektřina, postavili Fechner a v podrobnějším rozvinutí Weber názor, že v okruhu proudí vždy dva stejné proudy kladné a záporné elektřiny, pohybující se vedle sebe opačným směrem v kanálech, které leží mezi važitelnými molekulami látky. Při podrobném matematickém zpracování této theorie dochází Weber konečně také k tomu, že se nějaká, zde libovolná funkce musí násobit veličinou 1/r , což znamená „poměr elektrické jednotky k miligramu”,[5] (Wiedemann, „Lehre vom Galvanismus etc.”, 2. vyd., III, str. 569). Poměr k váhové míře může být ovšem zase jen váhový poměr. Tak dalece už tedy jednostranná empirie zapomněla pro počítání na myšlení, že zde nevažitelnou elektřinu dělá važitelnou a její váhu zanáší do matematických výpočtů.
Formule odvozené Weberem vyhovují jen v určitých mezích a zejména Helmholtz vyvodil z nich již před několika lety výsledky, které jsou v rozporu se zákonem o zachování energie. Proti Weberově hypothese protichůdného dvojitého proudu postavil K. Neumann roku 1871 jinou hypothesu, že se v elektrickém proudu pohybuje jenom jedna, na př. kladná elektřina, kdežto druhá, záporná, je pevně spojena s hmotou tělesa. Na to se váže u Wiedemanna poznámka: „Tuto hypothesu bychom mohli sjednotit s Weberovou, kdybychom k Weberovu předpokládanému dvojitému proudu opačně tekoucích elektrických mas ±½e připojili ještě proud neutrální elektřiny,[6] Navenek neúčinný, který by ve směru kladného proudu odnášel s sebou elektrické masy mas ±½e” (III, str. 577).
Tato věta je opět charakteristická pro jednostrannou empirii. Abychom elektřinu vůbec přiměli k proudění, rozložíme ji na kladnou a zápornou. Ale všechny pokusy vysvětlit proud s těmito dvěma substancemi narážejí na potíže. To platí jak o předpokladu, že po každé proudí jen jedna, tak i o tom, že proudí obě současně proti sobě, a konečně i o třetím, že proudí jen jedna a druhá stojí. Zastavíme-li se u posledního předpokladu, jak si vysvětlíme nevysvětlitelnou představu, že záporná elektřina, která je přece v leydenské láhvi dostatečně pohyblivá, v elektrickém proudu je najednou pevně spojena s hmotou? Velmi jednoduše. Necháme vedle kladného proudu + e, který proudí drátem napravo, a negativního – e, který proudí nalevo, protékat ještě proud neutrální elektřiny ±½e napravo. Nejprve předpokládáme, že obě elektřiny, aby vůbec proudily, musí být navzájem odděleny; abychom vysvětlili úkazy při proudění obou oddělených elektřin, předpokládáme, že mohou proudit také neodděleny. Nejprve učiníme nějaký předpoklad, abychom vysvětlili jistý úkaz, a při první potíži, na kterou narazíme, učiníme předpoklad druhý, který nám onen první přímo potírá. Jak asi musí vypadat filosofie, na kterou si mají tito páni právo stěžovat?
Vedle tohoto názoru o materiálnosti elektřiny vystoupil brzy jiný, podle něhož je elektřina interpretována jako pouhý stav těles, nějaká „síla”, nebo, jak bychom řekli dnes, zvláštní forma pohybu. Viděli jsme výše, že Hegel a později Faraday sdílejí tento názor. Od té doby, co objev mechanického ekvivalentu tepla definitivně odstranil představu jakési zvláštní „tepelné látky” a teplo se ukázalo molekulárním pohybem, bylo nejbližším krokem zacházet s elektřinou rovněž podle nových metod a pokusit se o stanovení jejího mechanického ekvivalentu. To se dokonale podařilo. Zejména pokusy Favra, Joula a Raoulta byl stanoven nejen mechanický a tepelný ekvivalent t. zv. „elektromotorické síly” galvanického proudu, nýbrž také její úplná ekvivalence s energii, uvolněnou chemickými procesy v galvanickém článku nebo spotřebovanou při elektrolytickém rozkladu. Stále neudržitelnějším se stává názor, že elektřina je zvláštní materiální fluidum.
Přitom analogie mezi teplem a elektřinou nebyla přece jenom ještě úplná. Galvanický proud se stále ještě odlišoval ve velmi podstatných bodech od vedení tepla. Stále ještě nebylo možno říci, co se pohybuje v elektricky aktivních tělesech. Předpoklad pouhého molekulárního kmitání, jako u tepla, se ukázal nedostatečným. Vzhledem k ohromné rychlosti elektřiny, přesahující rychlost světla[7], bylo těžké smířit se s představou, že se mezi molekulami tělesa pohybuje něco hmotného. Tady přicházejí nyní nejnovější theorie Clerka Maxwella (1864), Hankela (1865), Reynarda (1870) a Edlunda (1872) v souhlase s předpokladem, který již roku 1848 vyslovil jako domněnku Faraday, že elektřina je pohyb elastického media, pronikajícího všechen prostor a tudíž všechna tělesa, media, jehož jednotlivé diskretní částice se odpuzují nepřímo úměrně ke čtverci vzdálenosti, jinými slovy, že elektřina je pohyb etherových částiček a že molekuly tělesa se tohoto pohybu zúčastňují. V názoru na druh tohoto pohybu se jednotlivé theorie rozcházejí. Maxwellova, Hankelova a Reynardova theorie, které se opírají o novější výzkumy o vířivých pohybech, vysvětlují jej různým způsobem rovněž z víru, takže také víry starého Descarta přicházejí ve stále nových oblastech ke cti. Nebudeme se blíže zabývat podrobnostmi těchto theorií. Silně se navzájem rozcházejí a zažijí jistě ještě mnoho převratu. Ale jeden rozhodující pokrok patrně spočívá v jejich společném základním názoru: že elektřina je pohyb částic světelného etheru, pronikajícího všechnu važitelnou hmotu, a působící zpět na molekuly tělesa. Toto pojetí smiřuje obě předcházející. Podle nich se ovšem při elektrických jevech pohybuje něco hmotného, odlišného od važitelné hmoty. Ale toto hmotné něco není elektřina sama, která se ve skutečnosti spíše jeví jistou formou pohybu, i když ne bezprostředního, přímého pohybu važitelné hmoty. Tím, že etherová theorie ukazuje cestu, jak překonat primitivně neobratnou představu o dvou protikladných elektrických fluidech, dává za druhé vyhlídku na vysvětlení, co je vlastně hmotným substrátem elektrického pohybu, jaká je to věc, jejíž pohyb vyvolává elektrické úkazy.
Jeden rozhodující úspěch již etherová theorie zaznamenala. Jak známo, existuje nejméně jeden bod, kde elektřina mění přímo pohyb světla: otáčí jeho rovinu polarisace. Clerk Maxwell, opíraje se o svou theorii uvedenou výše, odvodil, že specifická dielektrická konstanta látky je rovna čtverci jejího indexu lomu světla. Boltzmann zkoumal dielektrické konstanty různých nevodičů a zjistil, že u síry, pryskyřice a parafinu je odmocnina z této konstanty rovna indexu lomu světla. Největší odchylka - u síry - činila jen 4 %. Tím byla speciálně Maxwellova etherová theorie experimentálně prokázána.
Bude to trvat ještě dlouhou dobu a stát ještě mnoho práce, než se podaří řadou nových pokusů vyloupnout pevné jádro z těchto jinak si navzájem odporujících hypothes. Do té doby, nebo do doby, než bude etherová theorie zatlačena nějakou zcela novou, je nauka o elektřině v té nepříjemné situaci, že musí používat terminologie, jejíž nesprávnost sama přiznává. Celá její terminologie spočívá stále ještě na představě dvou elektrických fluid. Stále ještě docela bez ostychu mluví o „elektrických masách proudících v tělesech”, o „oddělení obou elektřin v každé molekule” atd. Je to potíž, která z největší části, jak již řečeno, plyne nevyhnutelně ze současného přechodného stavu vědy, který však také při převládající jednostranné empirii právě v tomto oboru nemálo přispívá k udržení dosavadního myšlenkového zmatku.
Protiklad t. zv. statické neboli třecí elektřiny a dynamické elektřiny neboli galvanismu smíme jistě považovat za relativní od té doby, co jsme poznali, jak lze s třecími elektrikami vyrábět trvalý proud, a naopak, jak z galvanického proudu vyrábět t. zv. statickou elektřinu, nabíjet leydenské láhve atd. Necháme zde stranou statickou elektřinu stejně jako magnetismus, rozpoznané nyní jako určité odrůdy elektřiny. Theoretické vysvětlení zjevů sem náležejících bude nutno hledat za všech okolností v theorii galvanického proudu, a proto se budeme převážně zabývat jím.
Trvalý proud může být vyroben různými způsoby. Mechanický pohyb mas vyrábí přímo, třením, nejprve jen statickou elektřinu, trvalý proud jen za velikého mrhání energii; abychom jej alespoň z největší části převedli v elektrický pohyb, je nutné zprostředkování přes magnetismus, jako u známých magnetoelektrických strojů Gramma, Siemense a j. Teplo se může proměňovat přímo v elektrický proud, jako zejména na spájeném místě dvou různých kovů. Energie uvolněná chemickým působením, která se za normálních okolností projevuje ve formě tepla, přeměňuje se za určitých okolností v elektrický pohyb. Naopak, elektrický pohyb, pokud jsou pro to dány podmínky, přechází v každou jinou formu pohybu; v pohyb hmot, v malé míře přímo elektrodynamickým přitahováním a odpuzováním; ve velkém opět prostřednictvím magnetismu v elektromotorech; v teplo - všude v proudovém okruhu, pokud nejsou přivoděny jiné změny; v chemickou energii v elektrolytických lázních a voltametrech, zařazených do okruhu, kde proud rozkládá sloučeniny, které byly jiným způsobem marně napadány.
Při všech těchto proměnách platí zákon kvantitativní ekvivalence pohybu ve všech jeho formách. Neboli, jak to vyjadřuje Wiedemann: „Podle zákona o zachování síly mechanická práce, použitá nějakým způsobem k výrobě proudu, musí být ekvivalentní práci, spotřebované k vyrobení všech účinků proudu.”[8] Při přeměně pohybu hmot nebo tepla v elektřinu[*26] nenaskýtají se nám zde žádné potíže; v prvním případě je prokazatelně t. zv. „elektromotorická síla” rovna práci spotřebované na onen pohyb, v druhém případě „přímo úměrná absolutní teplotě na každém spájeném místě thermočlánku” (Wiedemann, III, str. 482), t. j. opět úměrná absolutně měřenému množství tepla na každém spájeném místě. Také pro elektřinu vyvinutou z chemické energie je tentýž zákon skutečně dokázán jako obecně platný. Ale zde se nám ― při nejmenším pro nyní platnou theorii ― nejeví věc tak jednoduchá. Všimněme si tohoto případu tedy poněkud blíže.
Jedna z nejkrásnější řady pokusů o změně forem pohybu, způsobené galvanickým článkem, jsou pokusy Favrovy (1857-58).[9] Do jednoho kalorimetru vložil Smeeův pětidílný článek; do druhého malý elektromotor, jehož hlavní osa a řemenice volně vyčnívaly k jakémukoli použití. Při každém uvolnění 1 g vodíku, respektive při rozpuštění 32,6 g zinku (vyjádřeno v gramech starého chemického ekvivalentu zinku, rovného poloviční dnes přijaté atomové váze 65,2), byly v článku zjištěny tyto výsledky:
A. Článek v kalorimetru spojen nakrátko, motor vyřazen z okruhu: vyvinuté teplo 18.682, resp. 18.674 tepelných jednotek.
B. Článek a motor spojeny do okruhu, ale motor udržován v klidu: teplo vyvinuté v článku 16.448. v motoru 2219, celkem tedy 18.667 tepelných jednotek.
C. Jako B., ale motor se otáčí, aniž však zvedá závaží: teplo v článku 13.888, v motoru 4769, celkem 18.657 kalorií.
D. Jako C., ale motor zdvíhá závaží a koná přitom mechanickou práci = 131,24 kgm: teplo v článku 15.427, v motoru 2947, celkem 18.374, ztráta proti hořejším 18.682 je 308 tepelných jednotek. Ale vykonaná mechanická práce 131,24 kgm, násobena 1000 (abychom gramy chemického výsledku převedli na kilogramy) a dělena mechanickým ekvivalentem tepla = 423,5 kgm[10], dává 309 tepelných jednotek, tedy přesně hořejší ztrátu, jako tepelný ekvivalent vykonané mechanické práce.
Ekvivalence pohybu při všech jeho proměnách je tedy pro elektrický pohyb - v mezích nevyhnutelných zdrojů chyb - pádně dokázána. A právě tak je dokázáno, že „elektromotorická síla” galvanického článku není nic jiného než chemická energie proměněná v elektřinu a že článek sám je jen zařízením, aparátem, který mění uvolňovanou chemickou energii v elektřinu, tak jako parní stroj mění přiváděné teplo v mechanický pohyb, aniž v obou případech stroj provádějící změnu přivádí ještě další energií sám ze sebe.
Ale zde vzniká tradičnímu způsobu uvažování potíž. Tento způsob uvažování připisuje totiž článku pro jeho kontakty, na stávající v něm mezí kapalinou a kovy, „elektrickou rozdělovací sílu”, která je úměrná elektromotorické síle, tedy pro daný článek representuje určité množství energie. V jakém poměru je nyní tento zdroj energie, inherentní podle tradičních představ článku jako takovému i bez chemické akce, tato elektrická rozdělovací síla, k energií uvolněné chemickým působením? A je-li zdroj energie nezávislý na chemickém působení, odkud pochází energie, kterou dodává?
Tato otázka je ve více nebo méně nejasné formě sporným bodem mezi kontaktní theorií založenou Voltou a chemickou theorií galvanického proudu, vzniklou krátce potom.
Kontaktní theorie vysvětlovala proud z elektrických napětí, vznikajících v článku při kontaktu kovů s jednou nebo více kapalinami a z jejich vyrovnání, resp. z vyrovnání napětí protikladných elektřin, takto rozdělených, ve vodivém okruhu. Chemické změny vznikající při tom považovala čistá kontaktní theorie za zcela podřadné. Naproti tomu tvrdil Ritter již roku 1805, že proud se může vytvořit jen tehdy, jestliže elektrody na sebe působily chemicky již před zapnutím. Všeobecně je starší chemická theorie Wiedemannem (I, str. 784) shrnuta tak, že podle ní tak zvaná kontaktní elektřina „může se objevit jen tehdy, když současně začíná účinkovat nějaké skutečné chemické působení dotýkajících se těles nebo alespoň nějaké porušení chemické rovnováhy, třebaže nespojené přímo s chemickými procesy, nějaká tendence k chemickému působení mezi oběma tělesy”.
Vidíme, že otázku zdroje energie galvanického proudu stavějí obě strany jen zcela nepřímo, ostatně tehdy tomu stěží mohlo být jinak. Volta a jeho nástupci považovali za zcela přirozené, že pouhý kontakt heterogenních těles může vyrábět trvalý proud, tedy konat bez náhrady určitou práci. Ritter a jeho přívrženci rozuměli stejně málo otázce, jak vlastně chemické působení dává článku schopnost vyrábět proud a jeho pracovní účinky. Je-li však pro chemickou theorii tento bod již dávno objasněn Favrem, Joulem, Raoultem a jinými, není tomu tak u kontaktní theorie. Ta stojí, pokud se udržela, stále ještě v podstatě na stupni, z něhož vyšla. Tak v dnešní nauce o elektřině stále ještě přežívají představy, které náležejí době dávno překonané, době, kdy jsme se musili spokojit nalezením nejbližší, na povrch vystupující zdánlivé příčiny pro nějaký účinek, lhostejno, zda přitom necháváme vznikat pohyb z ničeho, tedy představy, které přímo odporují zákonu o zachování energie. I když jsou tyto představy obrány o své nejspornější stránky, oslabeny, rozředěny, okleštěny a okrášleny, nemění to nic na věci: zmatek musí být jen tím větší.
Jak jsme viděli, prohlašuje sama starší chemická theorie proudu kontaktní vztahy v článku za naprosto nutné pro vytvoření proudu: tvrdí pouze, že tyto kontakty nevytvoří nikdy trvalý proud bez současného působení chemického. A ještě dnes se považuje za samozřejmé, že právě kontaktní zařízení článku tvoří aparát, s jehož pomocí se uvolněná chemická energie mění v elektřinu, a že záleží podstatně na těchto kontaktních zařízeních, zda a kolik chemické energie skutečně přejde v elektrický pohyb.
Wiedemann, jako jednostranný empirik, snaží se ze staré kontaktní theorie zachránit, co se zachránit dá. Sledujme ho při tom. Prohlašuje (I, str. 799):
„I když působení kontaktu chemicky indiferen1ních těles, na př. kovů, jak se dříve mělo za to, není nutné ani k theorii galvanického článku[11], ani není potvrzeno tím, že Ohm z něho odvodil svůj zákon, který by se dal odvodit i bez tohoto předpokladu, a že Fechner, který tento zákon experimentálně potvrdil, rovněž hájil kontaktní theorii, přece jen nemůže být vzbuzení elektřiny kontaktem kovů popíráno, alespoň podle pokusÚ, které máme dnes k disposici, i když dosažitelné výsledky trpí přitom vždy po kvantitativní stránce nevyhnutelnou nejistotou, neboť je nemožné udržet naprostou čistotu povrchů dotýkajících se těles.”
Vidíme, že kontaktní theorie se stala velmi skromnou. Připouští, že není naprosto nutná k vysvětlení proudu a že není dokázána ani theoreticky Ohmem, ani experimentálně Fechnerem. Dokonce připouští, že tak zvané fundamentální pokusy, o něž by se pak jedině ještě mohla opírat, mohou v kvantitativním ohledu přinést vždy jen nejisté výsledky, a nakonec na nás požaduje pouze jedno: abychom uznali, že kontaktem vůbec i když jen kovů! - vzniká elektrický pohyb.
Kdyby kontaktní theorie na tomto přestávala, nemohli bychom proti ní uvést ani slovo. Skutečně, je nutno bezpodmínečně přiznat, že při kontaktu dvou kovu vznikají elektrické jevy, pomocí nichž můžeme nechat sebou škubat preparovanou žabí nožičku, nabít elektroskop a vyvolat jiné zjevy. Zbývá již jen otázka: odkud pochází k tomu potřebná energie?
Abychom odpověděli na tuto otázku, budeme, podle Wiedemanna (I, str. 14), „uvažovat asi takto[12]: Přiblížíme-1i k sobě heterogenní kovové destičky A a B na malou vzdálenost, přitahují se následkem adhesních sil. Při vzájemném dotyku ztrácejí živou sílu pohybu, uděleného jim touto přitažlivostí. (Předpokládáme-li, že molekuly kovu neustále kmitají, mohla by zde také nastat změna jejich kmitáni se ztrátou živé síly, jestliže se při kontaktu heterogenních kovu dotýkají nesoučasně kmitající molekuly.) Ztracená živá síla se z největší části mění v teplo. Malé její části se však použije k tomu, aby jinak rozdělila dříve nerozdělené elektřiny. Jak jsme se už dříve zmínili, nabíjejí se snad[13] následkem nestejné přitažlivosti obou elektřin obě přiblížená tělesa stejným množstvím kladné a záporné elektřiny.”
Skromnost kontaktní theorie stále roste. Napřed se uznává, že mohutná elektrická rozdělovací síla, která má později vykonat takovou obrovskou práci, nemá v sobě samé žádnou vlastní energii a že nemůže fungovat, není-li jí přiváděna energie zvenčí. A pak je odkázána na více než trpasličí zdroj energie, živou sílu adhese, která vstupuje v činnost teprve na sotva měřitelné vzdálenosti a která dává tělesu urazit skoro neměřitelnou dráhu. Ale na tom nezáleží: ― tato síla nesporně existuje a rovněž nesporně pří kontaktu mizí. Ale i tento minimální zdroj energie dodává ještě příliš mnoho energie pro náš účel: velká část jeho se proměňuje v teplo a jen malá část slouží k vyvolám elektrické rozdělovací síly. Ačkoli se, jak známo, v přírodě vyskytuje mnoho případu, kdy neobyčejně malé nárazy vyvolávají m neobyčejně mohutné účinky, Wiedemann, jak se zdá, sám cítí, že jeho zdroj, stěží dodávající kapky energie: těžko stačí, a tak hledá nějaký jiný možný zdroj v předpokladu interference molekulárních kmitu obou kovu na dotykových plochách. Nehledě na jiné potíže, které se nám zde stavějí v cestu, Grove a Gassiot dokázali, že ke vzbuzení elektřiny dokonce vůbec není zapotřebí skutečného kontaktu, jak nám Wiedemann na předchozí stránce sám vypráví. Zkrátka, čím déle zkoumáme zdroj energie pro elektrickou rozdělovací sílu, tím více vysychá.
A přece neznáme až dosud nějaký jiný zdroj energie pro vzbuzení elektřiny při kontaktu kovů. Podle Naumanna („Allgemeine und Physikalische Chemie”, Heidelberg 1877, str. 657)[14] „proměňují kontaktní elektromotorické síly teplo v elektřinu”; považuje za „přirozený předpoklad, že schopnost těchto sil vzbuzovat elektrický pohyb závisí na množství tepla, jinými slovy, je funkcí teploty”, což prý bylo experimentálně dokázáno Le Rouxem. Také zde tápeme v nejistotě. Sáhnout k chemickým pochodům, které neustále v malé míře probíhají na kontaktních plochách, pokrytých vždy tenkými, pro nás vlastně neodstranitelnými vrstvičkami vzduchu a znečištěné vody, vysvětlit tedy vzbuzení elektřiny přítomností neviditelných a aktivních elektrolytu mezi kontaktními plochami, zakazuje nám zákon Voltovy řady kovu. Elektrolyt by musil ve vodivém kruhu vyrábět trvalý proud; elektřina pouhého dotyku kovu naproti tomu mizí, jakmile je okruh spojen. A zde přicházíme k vlastnímu hodu: zda a v jaké míře umožňuje „elektrická rozdělovací síla”, kterou Wiedemann sám nejprve omezil na kovy a prohlásil za neschopnou práce bez cizího zdroje energie, pak odkázal na opravdu mikroskopický zdroj energie, vysvětlit vytvoření trvalého proudu kontaktem chemický indiferentních těles.
Ve Voltově řadě jsou kovy seřazeny tak, že každý se chová vůči předcházejícímu elektronegativně a vůči následujícímu elektropositivně. Přiložíme-li tedy v tomto pořadí na sebe kousky kovu, třeba zinek, cín, železo, měď, platinu, pak můžeme na obou koncích získat elektrické napětí. Uspořádáme-li však tuto řadu kovu do vodivého uzavřeného okruhu, takže zinek a platina se dotýkají, napětí se okamžitě vyrovná a zmizí. „V každému uzavřeném okruhu látek, které patří do Voltovy řady, je tedy vytvoření trvalého proudu nemožné.”[15] Tuto větu podporuje Wiedemann ještě touto theoretickou úvahou: „Ve skutečnosti, kdyby v okruhu proudil trvalý elektrický proud, vyráběl by na kovových vodičích samých teplo, které by se nanejvýš rušilo ochlazením na místech dotyku kovu. Vyvolalo by to v každém případě nerovnoměrné rozdělení teploty; také bychom mohli tímto proudem bez jakéhokoli přívodu energie zvenčí trvale pohánět elektromotor, a tak konal práci, což je nemožné, neboť při pevném spojení kovů, na př. spájení, nemohou nastat ani na místech dotyku žádné zrněny, které by tuto práci kompensovaly.”[16]
A nestačí jen theoretický a experimentální důkaz, že kontaktní elektřina kovů nemůže sama vyrábět proud: uvidíme také, že se Wiedemann cítí nucen vytvořit zvláštní hypothesu, která její účinek odstraní i tam, kde by se v proudu snad přece jen uplatňovala.
Pokusme se tedy o jinou cestu, jak se dostat od kontaktní elektřiny k proudu. Představme si s Wiedemannem[17] „dva kovy - na příklad zinkovou a měděnou tyč - spojené na jednom konci; představme si dále, že jejich druhé konce jsou spojeny nějakým třetím tělesem, které nepůsobí elektromotoricky proti oběma kovům, nýbrž jenom vede protikladné elektřiny nashromážděné na jejich povrchu, takže se v něm vyrovnávají. Pak by elektrická rozdělovací síla neustále obnovovala dřívější rozdíl napětí, a tak by v okruhu vznikal trvalý proud, který by bez jakékoli náhrady konal práci, což je opět nemožné. - Podle toho tedy neexistuje těleso, které by jen vodilo elektřinu, bez elektromotorického působení vůči ostatním tělesům.” Nejsme tedy dále než předtím: nemožnost stvořit pohyb nám opět uzavírá cestu. Z kontaktu chemicky indiferentních těles, tedy' z vlastní kontaktní elektřiny, nedostaneme nikdy a nikde proud. Vraťme se tedy ještě jednou a zkusme třetí cestu, kterou nám ukazuje Wiedemann.
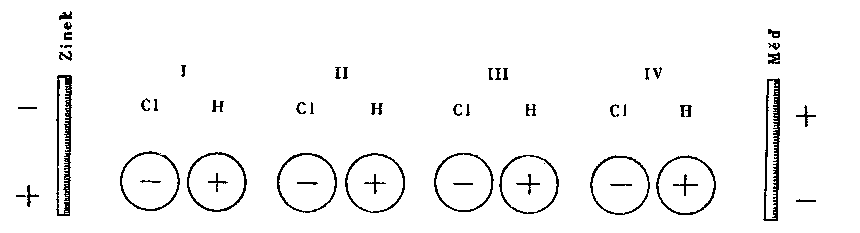
„Ponoříme-li jednu zinkovou a jednu měděnou destičku do kapaliny, která obsahuje tak zvanou binární sloučeninu a která se tedy může rozpadnout na dvě chemicky rozdílné části, které se navzájem úplně sytí, na př. zředěná kyselina solná (H + Cl) atd., pak se podle § 27 nabíjí zinek negativně, měď positivně. Při spojení obou kovů vyrovnávají se tyto elektřiny dotykovým místem, kterým tedy teče proud kladné elektřiny od mědi k zinku. Protože také elektrická rozdělovací síla, vznikající při kontaktu zmíněných kovů, dopravuje kladnou elektřinu ve stejném směru, účinky elektrických rozdělovacích sil se neruší jako v uzavřeném okruhu kovů. Vzniká tedy trvalý proud kladné elektřiny, který protéká v uzavřeném okruhu od mědi dotykovým místem k zinku a od zinku kapalinou zpět k mědi. Ještě se vrátíme k otázce (str. 34 a dále), do jaké míry skutečně jednotlivé zapojené elektrické rozdělovací síly spolupůsobí na vytvoření proudu. - Kombinace vodičů, která dává takový galvanický proud, se nazývá galvanický element, nebo také galvanický článek.” (I, str. 45).[18]
Zázrak byl tedy vykonán. Pouhou elektrickou rozdělovací silou, která podle samého Wiedemanna nemůže působit bez přívodu energie zvenčí, je zde vytvořen trvalý proud. A i kdybychom neměli k jeho vysvětlení nic jiného než hořejší citát z Wiedemanna, zůstává to ve skutečnosti úplným zázrakem. Co se zde dovíme o tomto pochodu?
1. Ponoříme-li zinek a měď do kapaliny, která obsahuje t. zv. binární sloučeninu, nabije se (podle § 27) zinek záporně a měď kladně. - Avšak v celém paragrafu 27 není ani slovo o nějaké binární sloučenině. Popisuje se tam pouze jednoduchý Voltův článek ze zinkové a měděné destičky, mezi nimiž leží plstěný kotouček navlhčený kyselou kapalinou, a vyšetřuje se pak bez jakékoli zmínky o chemických procesech - vznikající přitom staticko-elektrický náboj obou kovů. Tak zvaná bínární sloučenina je zde tedy vpašována zadními dvířky.
2. Co má být onou binární sloučeninou, zůstává úplnou záhadou. Okolnost, že se „může rozpadnout ve dvě chemicky rozdílné části, které se navzájem úplně sytí” (úplně sytí, když se . rozpadly? tj, by nás nanejvýš mohla naučit něčemu novému jen tehdy, kdyby se skutečně rozpadla. O tom se zde neříká ani slovo a musíme tedy prozatím předpokládat, že se nerozpadá, jako na př. u parafinu.
3. Je-li zinek v kapalině nabit negativně a měď positivně, uvedeme je (mimo kapalinu) v dotyk. Načež se „tyto elektřiny vyrovnají místem dotyku, jímž tedy protéká proud kladné elektřiny od mědi k zinku.” Opět se nedovídáme, proč teče jen „kladná” elektřina v jednom směru, a nikoli „záporná” elektřina v opačném směru. Nedovídáme se vůbec, co se děje se zápornou elektřinou, která byla přece až dosud stejně potřebná jako kladná; vždyť působení elektrické rozdělovací síly spočívalo právě v tom, aby se obě elektřiny volně postavily proti sobě. Nyní je záporná elektřina potlačena, jistým způsobem vyloučena a předpokládá se, jako by existovala jen kladná.
Pak se však na str. 51 říká pravý opak, neboť zde se „spojují elektřiny[19] v proud”, teče v něm tedy právě tak záporná elektřina jako kladná. Kdo nám pomůže z tohoto zmatku?
4. „Protože také při kontaktu uvedených kovů vznikající elektrická rozdělovací síla přenáší kladnou elektřinu ve stejném směru, účinky elektrické rozdělovací síly se neruší jako v uzavřeném okruhu kovů. Vzniká tedy trvalý proud” atd. ― To je trochu silné. Neboť, jak uvidíme, dokazuje nám Wíedemann o několik stránek dále (str. 52), že při „tvoření trvalého proudu... elektrická rozdělovací síla na místě dotyku kovů... musí být nečínná”[20], že tedy nejen vzniká proud, i když elektrická rozdělovací síla, místo aby přenášela kladnou elektřinu ve stejném směru, působí proti směru proudu, nýbrž že také v tomto případě není kompensována určitým podílem elektrické rozdělovací síly článku a tedy je opět neúčinná. Jak tedy může na str. 45 Wiedemann nechat spolupůsobit elektrickou rozdělovací sílu jako nutný faktor tvoření proudu, když ji na straně 52 po dobu tvoření proudu vyřazuje z činnosti, a to ještě vlastní k tomu účelu vytvořenou hypothesou?
5. „Vzniká tedy trvalý proud kladné elektřiny, který protéká v uzavřeném okruhu od mědi dotykovým místem k zinku a od zinku kapalinou zpět k mědi.” Avšak při takovém trvalém elektrickém proudu „bude jím samým vyráběno ve vodiči teplo,” také by jím mohl „být poháněn elektromotor a tak konána práce”, což však bez přívodu energie není možné. Poněvadž nám Wiedemann dosud ani písmenkem neprozradil, kde tato energie vzniká a odkud se bere, zůstává trvalý proud dosud právě tak čímsi nemožným jako v obou předcházejících zkoumaných případech.
Nikdo to necítí lépe než Wiedemann sám. Považuje tedy za vhodné přejít tak rychle, jak jen možno, přes četné choulostivé body těchto udivujících vysvětleni vzniku proudu a bavit čtenáře na několika stranách všelijakými elementárními anekdotami o thermických, chemických, magnetických a fysiologických účincích tohoto stále ještě záhadného proudu, při čemž dokonce výjimečně upadá do úplně populárního tónu. Pak zčista jasna pokračuje (str. 49): „Máme nyní vyšetřit, jakým způsobem fungují elektrické rozdělovací síly v uzavřeném okruhu dvou kovů a kapaliny, na př. zinku, mědi a kyseliny solné.
Víme, že se součásti binární sloučeniny (HCl), obsažené v kapalině, při protékání proudu dělí tím způsobem, že se jedna (H) uvolňuje na mědi a ekvivalentní množství druhé (Cl) na zinku, při čemž se Cl slučuje s ekvivalentním množstvím zinku na ZnCl.”[21]
Víme! Jestliže to víme, pak to určitě nevíme od Wiedemanna, který nám o tomto pochodu, jak jsme viděli, neprozradil ještě ani slovíčko. A dále, jestliže něco o tomto pochodu víme, pak je to ten fakt, že nemůže probíhat lak, jak to líčí Wiedemann.
Při tvoření molekuly HCl z plynného vodíku a chloru se uvolňuje 22.000 tepelných jednotek (Julius Thomsen). Abychom chlor vytrhli z jeho sloučeniny s vodíkem, musí být na každou molekulu HCl přivedeno zvenčí stejné množství energie. Odkud bere článek tuto energii? Wiedemannovo vysvětlení nám o tom nic neříká, poohlédněme se tedy sami.
Slučuje-li se chlor se zinkem na chlorid zinečnatý, uvolňuje se při tom značně větší množství energie, než je nutné k odtržení chloru od vodíku. (Zn, Cl,) uvolňuje 97.210, 2(H, CI) 44.000 tepelných jednotek (Julius Thomsen). A tím se stává pochod v článku vysvětlitelným. Není tedy, jak nám to vykládá Wiedemann uvolňován beze všeho dalšího vodík na mědi a chlor na zinku, „při čemž” se dodatečně a náhodně slučuje chlor se zinkem. Naopak: slučování zinku s chlorem je nejpodstatnější a základní podmínkou celého procesu, a pokud se tak neděje, budeme na mědi marně čekat na vodík.
Přebytek energie, který se uvolňuje při tvoření jedné molekuly ZnCl2 kromě energie, která se spotřebuje na uvolnění dvou atomů H ze dvou molekul HCl, proměňuje se v článku v elektrický pohyb a dodává celou „elektromotorickou sílu”, která se v proudovém okruhu skutečně vyskytuje. Není to tedy nějaká tajemná „elektrická rozdělovací síla”, která bez dosud prokázaného zdroje energie odtrhává vodík od chloru; je to celkový chemický pochod, probíhající v článku, který opatřuje všem „elektrickým rozdělovacím silám” a „elektromotorickým silám” v článku energii, nutnou k jejich existenci.
Konstatujeme tedy prozatím, že nám Wiedemannovo druhé vysvětlení proudu pomáhá právě tak málo s místa jako první, a pokračujeme v textu.[22]
„Tento proces dokazuje, že úloha binární sloučeniny mezi kovy nespočívá pouze v jednoduchém převažujícím přitahování celé její hmoty k jedné nebo druhé elektřině, jako je tomu u kovů, nýbrž že zde přistupuje ještě zvláštní působení jejích složek.. Protože složka Cl se odštipuje tam, kde do kapaliny ustupuje proud kladné elektřiny, složka H tam, kde vstupuje záporná elektřina, předpokládáme[23], že každý ekvivalent chloru v sloučenině HCl je nabit určitým množstvím záporné elektřiny, která způsobuje jeho přitahování vstupující kladnou elektřinou. To je elektronegativní součást sloučeniny. Právě tak musí být ekvivalent H nabit kladnou elektřinou a představovat tak elektropositivní součást sloučeniny. Tyto náboje by se mohly při slučování H a Cl vytvořit úplně stejně jako při kontaktu zinku a mědi. Protože je sloučenina HCl sama neelektrická, musíme podle toho předpokládat, že v ní atomy positivní a negativní součásti obsahují stejné množství kladné a záporné elektřiny.
Je-li nyní do zředěné kyseliny solné ponořena destička zinková a destička měděná, pak se můžeme domnívat, že zinek má silnější přitažlivost k její elektronegativní součásti (Cl) než k elektropositivní (H). V důsledku toho by se uspořádaly molekuly kyseliny solné, dotýkající se zinku, tak, že se jejích elektronegativní součásti obrátí k zinku, elektropositivní k mědi. Protože takto seřazené součásti působí svým elektrickým přitahováním na části následující molekuly HCl, srovná se celá řada molekul mezi zinkovou a měděnou destičkou jako na obrázku 10:

Kdyby působil druhý kov na positivní vodík tak, jako působí zinek na negativní chlor, bude tím seřazení podporováno. Kdyby působil opačně, ale slaběji, zůstává při nejmenším směr tohoto seřazení nezměněn.
Influenčním působením záporné elektřiny elektronegativní součásti Cl přiléhající k zinku byla by[24] na zinku rozložena elektřina tak, že by ty jeho části, které leží v blízkosti Cl nejbližšího atomu[25] kyseliny, byly nabity kladně, dále ležící části záporně. Právě tak by byla v mědi nahromaděna záporná elektřina v blízkosti elektropositivní součásti (H) přiléhajícího atomu kyseliny solné, kladná elektřina zatlačena k vzdálenějším částem.
Pak by se kladná elektřina v zinku spojila se zápornou elektřinou nejbližšího atomu Cl a atom Cl sám by se spojil se zinkem [na neelektrické ZnCl2][26]. Elektropositivní atom H, který byl předtím spojen s oním atomem Cl, sloučil by se s atomem Cl, obráceným k němu, za současného spojení elektřin obsažených v těchto atomech; podobně by se sloučil[27] H druhého atomu HCl s Cl třetího atomu atd.; až by se konečně na mědi uvolnil atom H, jehož kladná elektřina by se spojila s rozdělenou negativní elektřinou mědi, takže by unikl v neelektrickém stavu.” Tento proces „by se tak dlouho opakoval, až by odpuzování elektřin nahromaděných na elektrodách vůči elektřinám součástí kyseliny solné, obrácených k nim, právě vyvažovalo chemickou přitažlivost obou součástí vůči kovům. Jsou-li však obě elektrody navzájem vodivě spojeny, volné elektřiny kovových destiček se navzájem spojí a právě uvedené procesy mohou nastat znovu. Tímto způsobem by tedy vznikl trvalý proud elektřiny. - Je zřejmé, že přitom nastává neustálá ztráta živé síly, když se součásti binární sloučeniny, cestující ke kovům, pohybují určitou rychlostí a pak se zastavují, buď tím, že tvoří sloučeninu (ZnCl), nebo tím, že volně unikají (H). (Poznámka [Wiedemannova]: Protože se zisk živé síly při rozštěpení součástí Cl a H … opět vyrovnává ztrátou živé síly při jejich slučování se součástmi nejbližších atomů, je možno vliv tohoto procesu zanedbat.) Tato ztráta živé síly je ekvivalentní množství tepla, které se uvolňuje při viditelně probíhajícím chemickém procesu, tedy v podstatě při rozpouštění jednoho ekvivalentu zinku v zředěné kyselině. Této hodnotě musí být rovnocenná práce, spotřebovaná na rozdělení elektřin. Jestliže se tedy elektřiny v proudu spojí, musí během rozpouštění jednoho ekvivalentu zinku a vyloučení jednoho ekvivalentu vodíku z kapaliny v celém vodivém okruhu vzniknout práce (ať už ve formě tepla, nebo ve formě působení navenek), která je rovněž ekvivalentní množství tepla, odpovídajícímu onomu chemickému procesu.”
„Předpokládejme - mohly by - museli bychom předpokládat - mohli bychom se domnívat - byla by rozdělena - nabily by se -” atd. atd. Samé domněnky a podmiňovací způsoby, ze kterých lze s určitostí vylovit jenom tři faktická tvrzení: za prvé, že spojení zinku s chlorem se nyní prohlašuje za podmínku uvolnění vodíku; za druhé, jak se teď na konci a jakoby mimochodem dovídáme, že uvolněná při tom chemická energie je zdrojem, a to výhradním zdrojem vší energie nutné k vytvoření proudu; a za třetí, že toto vysvětlení proudu prudce odporuje oběma předcházejícím vysvětlením tak, jako ona sobě navzájem.
Dále se říká:
„Při tvoření trvalého proudu se tedy může uplatnit jedině a výhradně[28] ta elektrická rozdělovací síla, která pochází od nestejného přitahování a polarisace atomů binární sloučeniny v elektrolytu článku kovovými elektrodami; elektrická rozdělovací síla na kontaktním místě obou kovů, kde už nemůže probíhat žádná mechanická změna, musí naproti tomu být nečinná.[29] Že tato síla, když snad působí proti elektromotorickému nabití kovů kapalinou (jako na př. při ponoření cínu a olova do roztoku cyankali), není kompensována určitým podílem rozdělovací síly na místech dotyku kovů a kapaliny, dokazuje zmíněná dokonalá úměrnost celkové elektrické rozdělovací síly (a elektromotorické síly) ve vodivém okruhu se zmíněným tepelným ekvivalentem chemických procesů. Musí být tedy neutralisována jiným způsobem. To se stane nejjednodušeji za předpokladu, že při dotyku elektrolytu s kovy je vyráběna elektromotorická síla dvojím způsobem. Jednou nestejným přitahováním hmot kapaliny jako celku k jedné nebo druhé elektřině; anebo pak nestejným přitahováním kovů k součástem[30] kapaliny nabitým opačnými elektřinami. Následkem prvního, nestejného přitahování hmot k elektřinám chovaly by se kapaliny zcela podle zákona Voltovy řady kovů a v uzavřeném okruhu by nastala úplná neutralisace elektrických rozdělovacích sil (a elektromotorických sil) na nulu; druhé, chemické[31] působení... by dodávalo naproti tomu samo všechnu elektrickou rozdělovací sílu nutnou pro vytvoření proudu a jí odpovídající elektromotorickou sílu” (I, str. 52, 53).
Tím byl tedy šťastně odstraněn poslední zbytek kontaktní theorie z tvoření proudu a současně také poslední zbytek prvního vysvětlení vzniku proudu, uvedeného na str. 45. Konečně se bez výhrad přiznává, že galvanický článek je jednoduchý aparát k přeměně uvolňované chemické energie v elektrický pohyb, v t. zv. elektrickou rozdělovací sílu a v elektromotorickou sílu, zcela tak, jako parní stroj je aparát na proměnu tepelné energie v mechanický pohyb. V obou případech tvoří aparát jen podmínky pro uvolnění a další proměny energie, ale sám ze sebe žádnou energii nedodává. Když je toto jednou stanoveno, zbývá nám ještě blíže prozkoumat třetí versi Wiedemannova vysvětlení vzniku proudu.
Jak jsou znázorňovány proměny energie ve vodivém okruhu? Je jasné, říká Wiedemann, že v článku „nastává neustálá ztráta živé síly, když součásti binární sloučeniny, cestující ke kovům, se pohybují určitou rychlostí a pak se buď při tvoření sloučeniny (ZnCl2) , nebo tím, že volně unikají (H), zastaví. Tato ztráta živé síly je ekvivalentní množství tepla, které se uvolňuje při viditelně probíhajícím chemickém procesu, tedy v podstatě při rozpouštění jednoho ekvivalentu zinku v zředěné kyselině solné.”
Za prvé, pokud proces v článku probíhá v čisté formě, neuvolňuje se při rozpouštění zinku žádné teplo; uvolněná energie se proměňuje přímo v elektřinu a teprve z ní odporem celého okruhu opět v teplo.
Za druhé je živá síla poloviční součin hmoty a čtverce rychlosti. Hořejší věta by tedy zněla: Energie, uvolněná při rozpouštění jednoho ekvivalentu zinku, se rovná tolika a tolika kaloriím, a je současně rovnocenná polovičnímu součinu hmoty iontů s čtvercem rychlosti, jíž se pohybuji ke kovům. Takto vyslovena je tato věta zřejmě chybná. Živá síla, objevující se při putování iontů, je daleko vzdálena tomu, aby byla rovnocenná energii, uvolněné při chemickém procesu.[*27] Kdyby tomu tak bylo, nebyl by možný žádný proud, neboť by nezbyla žádná energie pro proud v ostatním okruhu. Proto se ještě připojuje poznámka, že ionty jsou zastaveny buď při tvoření sloučeniny, nebo tím, že volně unikají. Má-li však ztráta živé síly zahrnovat i tyto změny energie, probíhající při obou procesech, pak jsme se tím spíše dostali do slepé uličky. Neboť jsou to právě tyto dva procesy, vzaté dohromady, kterým děkujeme za celou uvolněnou energii, takže zde naprosto nemůžeme mluvit o nějaké ztrátě živé síly, nanejvýše o jejím získání.
Je tedy jasné, že Wiedemann si při této větě sám nic určitého nepředstavoval, spíše je „ztráta živé síly” jakýsi deus ex machina[32], který mu má umožnit fatální skok od staré kontaktní theorie k chemickému vysvětlení proudu. A skutečně, „ztráta živé síly” vykonala svou povinnost a může jít; od nynějška je chemický pochod v článku nesporně uznáván za jediný zdroj energie při vzniku proudu a jediná ještě zbývající starost našeho autora je, jak se zbavit - pokud možno nějakým slušným způsobem - posledního zbytku elektřiny, vznikající při kontaktu chemicky indiferentních těles, totiž elektrické rozdělovací síly, působící na místě styku obou kovů.
Čteme-li hořejší Wiedemannovo vysvětlení vzniku proudu, zdá se nám, že máme před sebou kus té apologetiky, s kterou vystoupili skoro před čtyřiceti lety pravověrní nebo polopravověrní theologové proti filologicko-historické kritice bible, podané Straussem, Wilkem, Brunem Bauerem a j. Metoda je v obou případech stejná. Musí být, neboť v obou případech jde o záchranu zděděné tradice před myslící vědou. Výhradní empirie, které je dovoleno myslet nanejvýš ve formě matematického počítání, se domnívá, že pracuje jen s nepochybnými skutečnostmi. Ve skutečnosti však operuje hlavně s tradičními představami, většinou překonanými produkty myšlení svých předchůdců, jako jsou kladná a záporná elektřina, elektrická rozdělovací síla, kontaktní theorie. Slouží jí za základnu pro nekonečné matematické výpočty, v nichž se pro přesnost matematických vzorců snadno zapomíná na hypothetickou povahu předpokladů. Jak skepticky se tento druh empirie staví k výsledkům současného myšlení, tak důvěřivě se chová k výsledkům myšlení svých předchůdců. Dokonce i experimentálně zjištěné skutečnosti se jí ponenáhlu staly neodlučnými od příslušných tradičních výkladů; nejjednodušší elektrický jev je ve svém znázornění zfalšován, na př. vpašováním dvou elektřin; tato empirie nemůže už správně popisovat skutečnosti, neboť tradiční výklad proniká i do popisu. Zkrátka: máme zde na poli nauky o elektřině tak vyvinutou tradiCl jako v theologii. A protože v obou případech výsledky nového bádání, zjištění dosud neznámých nebo sporných faktů, a z toho nutně plynoucí theoretické vývody nemilosrdně potírají staré tradice, ocítají se obránci těchto tradic v těžkém postavení. Musí se uchylovat k nejrůznějším úskokům, neudržitelným výmluvám, k zatušovávání nesmiřitelných rozporů a ocitají se nakonec sami ve zmatku rozporů, z něhož není pro ně žádné východisko. Je to víra ve starou theorii elektřiny, která Wiedemanna zamotává do nejbeznadějnějších rozporů se sebou samým, prostě beznadějný pokus racionalisticky sloučit staré vysvětlení proudu „kontaktní silou” s novější theorií o uvolňování chemické energie.
Někdo nám snad namítne, že hořejší kritika Wiedemannova vysvětlení proudu spočívá na lpění na slovech; jestliže se Wiedemann z počátku vyjadřuje poněkud nedbale a nepřesně, pak nakonec přece jen dává správné vysvětlení, souhlasící s poučkou o zachování energie, a tím všechno napravuje. Naproti tomu zde podáváme jiný příklad, jeho popis pochodu v článku: zinek, zředěná kyselina sírová, měď.
„Spojíme-li však obě destičky drátem, vzniká galvanický proud... Z vody[33] zředěné kyseliny sírové se vylučuje elektrolytickým procesem na mědi jeden ekvivalent vodíku, který uniká v bublinkách. Na zinku se tvoří jeden ekvivalent kyslíku, který oxyduje zinek na kysličník zinečnatý, a ten se rozpouští v obklopující ho kyselině na síran zinečnatý.” (I, str. 593.)
Abychom vyloučili plynný kyslík a vodík z vody, k tomu je zapotřebí na každou molekulu vody energie 68.924 tepelných jednotek. A odkud se nyní bere energie v našem článku? „Elektrolytickým procesem.” A odkud ji bere elektrolytický proces? Žádná odpověď.
Avšak Wiedemann nám nevypráví jednou, nýbrž nejméně dvakrát (I, str. 472 a 614), že „voda podle nejnovějších zkušeností [při elektrolyse] není vůbec rozkládána”, nýbrž v našem případě se rozkládá kyselina sírová H2SO4 a to na jedné straně na H2 na druhé na SO3+O, při čemž H2 a O mohou za jistých okolnosti uniknout jako plyn. Tím se však mění celá povaha procesu. H2 v H2SO4 je přímo nahrazováno dvojmocným zinkem a tvoří se síran zinečnatý ZnSO4. Na jedné straně zůstává H2 na druhé SO3+O. Oba plyny unikají v poměru, v němž tvoří vodu; SO3, se spojuje s vodou roztoku H2O zpět na H2SO4, t. j. kyselinu sírovou. Při tvorbě ZnSO4 se však vyvíjí množství energie, které stačí nejen k vy těsnění a uvolnění vodiku z kyseliny sírové, nýbrž ještě zanechává značný přebytek, který vede v našem případě ke vzniku elektrického proudu. Zinek tedy nečeká, až mu elektrolytický proces dá k disposicí volný kyslík, aby se teprve pak okysličil a rozpustil v kyselině. Vstupuje přímo do procesu, který nastává teprve účasti zinku.
Vidíme zde, jak zastaralým představám o kontaktu přicházejí na pomoc zastaralé představy chemické. Podle nejnovějšího názoru je sůl kyselina, v níž byl vodík nahrazen kovem. Pochod, který je zkoumán, potvrzuje tento názor: přímé vy těsnění vodíku kyseliny zinkem úplně vysvětluje proměnu energie. Starší názor, podle něhož se řídí Wiedemann, považuje sůl za sloučeninu kysličníku kovu a kyseliny a mluví proto místo o „síranu zinečnatém” o „kyselino-sírovém kysličníku zinečnatém”.
Abychom se však v našem článku dostali od zinku a kyseliny sírové ke kyselino-sírovému kysličníku zinečnatému, musí být zinek nejprve oxydován. Abychom zinek dostatečně rychle oxydovali, musíme mít volný kyslík. Abychom se dostali k volnému kyslíku, musíme předpokládat, protože se na mědi objevuje vodík, že se voda rozkládá. Abychom rozložili vodu, potřebujeme ohromnou energii. Jak k ní přijít? Jednoduše „elektrolytickým procesem”, který se sám opět nemůže rozběhnout, pokud se nezačne tvořit jeho konečný produkt, „kyselinosírový kysličník zinečnatý”. Dítě rodí matku.
Také zde je tedy u Wiedemanna celý proces úplně převrácen a postaven na hlavu. A to proto, že Wiedemann hází pasivní a aktivní elektrolysu, dva přímo protikladné procesy, bez okolků přímo do jednoho pytle jako elektrolysu vůbec.
Až dosud jsme zkoumali, co se děje v článku, t. j. proces, při němž se chemickým působením uvolňuje přebytek energie a zařízením článku proměňuje v elektřinu. Tento proces může být, jak známo, také obrácen: elektřina trvalého proudu, vyrobená v článku z chemické energie, může být opět proměněna zpět v chemickou energii v elektrolytické lázni, zařazené do okruhu. Oba procesy jsou zjevně protikladné; považujeme první za elektrochemický, druhý za chemicko-elektrický. Oba mohou v témže okruhu probíhat na těchže látkách. Tak může článek, složený z plynných prvků, jehož proud je vyráběn slučováním vodíku a kyslíku ve vodu, dodávat v elektrolytické lázni zařazené do okruhu vodík a kyslík v témže poměru, v němž tyto prvky tvoří vodu. Běžné pojetí shrnuje tyto dva protikladné procesy pod jeden výraz: elektrolysa, a nerozlišuje ani mezi aktivní a pasivní elektrolysou, ani mezi aktivním elektrolytem, elektrolytem článku, a pasivním elektrolytem, rozkládaným roztokem. Tak pojednává Wiedemann na 143 stránkách všeobecně o elektrolyse a připojuje pak na konci několik poznámek o „elektrolyse v článku”, z nichž pochody ve skutečných článcích zabírají jen nejmenší část 17 stránek tohoto oddílu. Také v následující „theorii elektrolysy” není o tomto protikladu mezi článkem a elektrolytickou lázní ani zmínka, a kdo by v následující kapitole „Vliv elektrolysy na odpor vodičů a na elektromotorickou snu ve vodivém okruhu” hledal nějaké respektování proměn energie v okruhu, ten by byl trpce zklamán. Všimněme si nyní tohoto neodolatelného „elektrolytického pochodu”, který bez viditelného přívodu energie dovede oddělit H2 od O a který v těchto oddílech knihy hraje tutéž úlohu jako předtím tajuplná „elektrická rozdělovací síla”.
„Vedle primárního, čistě elektrolytického[34] procesu oddělení iontů vyskytuje se ještě mnoho jiných sekundárních, čistě chemických[35] procesů, úplně nezávislých na primárním procesu, vlivem iontů vyloučených proudem. Toto působení se může týkat látky elektrod i rozkládaných látek, v roztocích také rozpustidla” (I, str. 481). - Vraťme se k našemu hořejšímu článku: zinek a měď v zředěné kyselině sírové. Zde jsou, podle vlastního prohlášení Wiedemannova, oddělené ionty H2 a O vody. Proto je oxydace zinku a tvoření ZnSO4 procesem sekundárním, nezávislým na elektrolytickém procesu, čistě chemickým procesem, ačkoli teprve jím se stává možným onen primární proces. Všimněme si poněkud podrobněji zmatku, který z tohoto převrácení skutečného průběhu musí vzniknout.
Podívejme se nejprve na t. zv. sekundární procesy v elektrolytické lázni, z nichž nám Wiedemann uvádí několik příkladů[*28] (str. 481, 482):
I. Elektrolysa Na2SO4 rozpuštěného ve vodě. Ten se „rozpadá... na jeden ekvivalent SO3 + O... a na jeden ekvivalent Na... Ale reaguje s vodou roztoku a vylučuje z ní jeden ekvivalent H, za tím co se tvoří jeden ekvivalent louhu sodného (NaOH) a rozpouští se v okolní vodě”. Rovnice je:
Na2SO4 + 2H2O = O + SO3 + 2NaOH + 2H.
V tomto příkladu skutečně může být rozklad:
Na2SO4 = Na2 + SO3 + O
chápán jako primární, elektrochemický, a další proměna:
Na2 + 2H2O = 2NaOH + 2H
jako sekundární, čistě chemický proces. Ale tento sekundární pochod probíhá bezprostředně na té elektrodě, kde se objevuje vodík; uvolněné přitom velmi značné množství energie (111.810 tepelných jednotek pro Na, O, H, aq. podle Julia Thomsena) se proto, alespoň z největší části, mění v elektřinu a jen část přechází v elektrolytické lázni bezprostředně v teplo. Totéž se může stát s chemickou energií, uvolněnou přímo nebo primárně v článku. Množství energie takto získané a proměněné v elektřinu se však odčítá od toho, které musí proud dodávat k nepřetržitému rozkladu Na2SO4.Vypadá-li proměna sodíku v louh v prvním okamžiku celého procesu jako sekundární proces, stává se v druhém okamžiku podstatným faktorem celého, pochodu a přestává být tedy sekundární.
Dále se však odehrává v elektrolytické lázni ještě třetí proces: SO3 - pokud nevstupuje v sloučeninu s kovem kladné elektrody, čímž se opět uvolňuje energie - se slučuje s vodou na H2SO4 kyselinu sírovou. Tato změna však neprobíhá bezprostředně na elektrodě, a proto se uvolněné množství energie (21.230 tepelných jednotek podle Julia Thomsena) zcela nebo z větší části proměňuje přímo v elektrolytické lázni v teplo a odevzdává nanejvýš jen nepatrnou část, ve formě elektřiny, proudu. O jediném skutečně sekundárním procesu, který probíhá v elektrolytické lázni, se tedy Wiedemann nezmiňuje.
II. „Elektrolysujeme-li roztok modré skalice [CuSO4.+ 5H2O] mezi kladnou elektrodou měděnou a zápornou platinovou, vylučuje se - při současném rozkladu okyselené vody v témže okruhu - na záporné platinové elektrodě na jeden ekvivalent vody jeden ekvivalent mědi; na kladné elektrodě by se měl” objevit jeden ekvivalent SO4; ten se však slučuje s mědí elektrody na jeden ekvivalent CuSO4, který se rozpouští ve vodě elektrolysovaného roztoku.”
V moderním chemickém znázornění si musíme proces představit takto: na platině se usazuje měď; uvolněný SO4 který jako takový nemůže existovat, rozpadá se na SO3 + O, při čemž O volně uniká; SO3, přejímá vodu z elektrolysovaného roztoku a tvoří kyselinu sírovou H2SO4 která se opět spojuje s mědí elektrody na CuSO4 za současného uvolnění H2. Máme zde přesně řečeno tři pochody: 1. oddělení Cu a SO4; 2. SO3 + O + H2O = H2SO4 + O; 3. H2SO4 + Cu = H2 + CuSO4. Bylo by při rozené považovat první proces za primární, oba ostatní za sekundární. Ptáme-li se však po proměnách energie, shledáme, že první proces je plně kompensován částí třetího: odtržení mědi od SO4 je kompensováno jejich opětným spojením na druhé elektrodě. Jestliže nepřihlížíme k energii, nutné na převedení mědi od jedné elektrody k druhé, a rovněž k nevyhnutelné, přesně neurčitelné ztrátě energie v článku proměnou v teplo, máme zde případ, kdy t. zv. primární pochod neubírá proudu žádnou energii. Proud dodává energii výlučně k umožnění od dělení H2 a O, k tomu ještě nepřímého, které se jeví jako skutečný chemický resultát celého procesu - tedy k provedení sekundárního nebo dokonce terciárního procesu.
V obou hořejších příkladech, jakož i v jiných případech má rozlišování mezi primárními a sekundárními procesy nesporně jisté relativní oprávnění. Tak se v obou případech zdánlivě rozkládá voda a prvky vody se vylučují na protilehlých elektrodách. Protože podle nejnovějších poznatků se absolutně čistá voda maximálně přibližuje ideálu nevodiče, tedy také neelektrolytu, je důležité dokázat, že v tomto a podobných případech není tedy elektrochemicky rozkládána sama, voda, nýbrž že prvky vody jsou vylučovány z kyseliny, při jejímž tvoření musí ovšem spolupůsobit voda roztoku.
III. „Elektrolysujeme-li ve dvou trubicích tvaru U současně... kyselinu solnou [HCl + 8H2O] a použijeme-li v jedné trubici jako kladné elektrody zinku, v druhé mědi, pak se v první trubici rozpustí zinku 32,53, v druhé mědi 2 x 31,7.”[36]
Necháme měď prozatím stranou a věnujme se zinku. Jako primární pochod zde platí rozklad HCl, jako sekundární rozpuštění Zn.
Podle tohoto pojetí přivádí proud zvenčí do elektrolytické lázně energii nutnou k oddělení H a Cl, a jakmile je rozklad proveden, slučuje se Cl se Zn; přitom se uvolňuje energie, která se odčítá od energie nutné k oddělení H a Cl; proudu tedy stačí přivádět rozdíl. Až dosud všechno krásně souhlasí; všimneme-li si však obou množství energie blíže, zjistíme, že energie uvolněná při tvoření ZnCl je větší než energie spotřebovaná při rozkladu 2HCl. Proud tedy nemusí přivádět žádnou energii, nýbrž naopak, sám energii dostává. Nemáme tedy před sebou žádný pasivní elektrolyt, nýbrž aktivní elektrolyt - elektrolytický roztok, žádnou elektrolytickou lázeň, nýbrž článek, který zesiluje baterii článků vytvářející proud o nový prvek. Proces, který jsme měli považovat za sekundární, se stává naprosto primárním, stává se zdrojem energie celého procesu a činí jej nezávislým na přiváděném proudu.
Vidíme zde jasně, že zdroj celého zmatku v tomto theoretickém výkladu je v tom, že Wiedemann vychází z elektrolysy, ať je aktivní nebo pasivní, ať je to článek nebo elektrolytická lázeň, jemu je to jedno: „felčar jako felčar”, jak pravil starý major k jednoročnímu dobrovolníkovi, doktorovi filosofie.” [37] A protože elektrolysa se v elektrolytické lázni mnohem snáze studuje než v článku, vychází. Wiedemann skutečně z elektrolytické lázně, dělá procesy probíhající v ní, jejich částečně oprávněné rozdělení na primární a sekundární, měřítkem úplně obrácených pochodů v článku a ani přitom nepozoruje, že se mu elektrolytická lázeň pod rukama proměňuje v článek. Proto může vyslovit větu: „Chemická afinita vyloučených látek vůči elektrodám je bez vlivu na vlastní elektrolytický proces” (I, str. 471), větu, která v této absolutní formě je, jak jsme právě viděli, úplně chybná. Odtud pak také pochází trojitá theorie vzniku proudu: za prvé stará tradiční theorie na základě čistého kontaktu; za druhé theorie s již abstraktněji pojatou elektrickou rozdělovací silou, která nevysvětlitelným způsobem opatřuje energii sobě nebo „elektrolytickému procesu”, energii, která v článku odtrhne od sebe H a Cl a mimo to ještě tvoří proud; a konečně moderní, chemicko-elektrická theorie, která vidí zdroj energie v součtu chemických působení v článku. Jako nepozoruje, že druhé vysvětlení potírá první, právě tak netuší, že třetí vylučuje druhé. Naopak, poučka o zachování energie je u něho zcela vnějšně připojena na tradiční theorie, jako věšíme jednu geometrickou poučku na dřívější. Ani tušení o tom, že tato poučka vede nutně k revisi celého tradičního způsobu nazírání jak v tomto oboru přírodovědy, tak i v ostatních. Proto se Wiedemann omezuje na to, že poučku o zachování energie při vysvětlení proudu pouze konstatuje a pak ji klidně odkládá, aby se ji zabýval až zcela na konci knihy v kapitole o účincích proudu. Dokonce i v theorii vzbuzení elektřiny kontaktem (I, 781 a dále) nehraje zachováni energie žádnou úlohu při vysvětlení hlavní věci a je jí jen příležitostně použito k vysvětlení vedlejších bodů: je a zůstává „sekundárním procesem”.
Vraťme se zpět k hořejšímu příkladu III. Tam byla ve dvou trubicích tvaru U týmž proudem elektrolysována kyselina solná, ale v jedné byl kladnou elektrodou zinek, v druhé měď. Podle Faradayova základního elektrolytického zákona rozloží tentýž galvanický proud v každé elektrolytické lázni ekvivalentní množství elektrolytu a množství látek vyloučených na obou elektrodách jsou rovněž v poměru svých ekvivalentů (I, str. 470). Nyní se zjistilo, že v hořejším případě se v první trubiCl rozpustilo zinku 32,53, v druhé mědi 2 x 31,7. „Není to přesto žádný důkaz,” pokračuje Wiedemann, „pro ekvivalenci těchto hodnot. Tyto hodnoty jsou naměřeny jen při slabých proudech, když se tvoří chlorid zinečnatý na jedné straně... a chlorid měďný na druhé straně. Pro silnější proudy klesne množství rozpuštěné mědi při tomtéž množství rozpuštěného zinku… až na 31,7, při čemž se tvoří stále více chloridu měďnatého.”
Zinek, jak známo, tvoří jen jednu sloučeninu s chlorem, chlorid zinečnatý ZnCl2; měď naproti tomu dvě, chlorid měďný CuCl2 a chlorid měďnatý Cu2Cl2. Původ rozporu je tedy v tom, že slabý proud na každé dva atomy chloru odtrhne od elektrody dva atomy mědi, které jednou svou valenční jednotkou zůstávají spojeny, kdežto zbývající dvě valence se sloučí s dvěma atomy chloru:
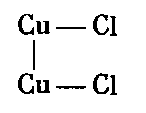
Když však proud zesílí, odtrhne atomy mědi zcela od sebe a každý z nich se spojí s dvěma atomy chloru:
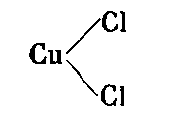
Při proudech střední síly se tvoří obě sloučeniny vedle sebe. Je to tedy pouze síla proudu, která podmiňuje tvoření té či oné sloučeniny, a proto je tento proces ve své podstatě elektrochemický, pokud má toto slovo vůbec nějaký smysl. Přesto Wiedemann kategoricky prohlašuje tento proces za sekundární, a tedy ne elektrochemický, nýbrž čistě chemický.
Hořejší pokus pochází od Renaulta (1867) a patří k celé řadě podobných pokusů, při nichž byl tentýž proud veden v trubici tvaru U roztokem kuchyňské soli (kladná elektroda zinek) a v jiném článku rozličnými elektrolyty s rozličnými kovy jako kladnými elektrodami. Přitom množství ostatních kovů rozpuštěná na jeden ekvivalent zinku se značně lišila a Wiedemann udává výsledky celé řady pokusů, které jsou však chemicky většinou samozřejmé a naprosto nemohou dopadnout jinak. Tak byly na jeden ekvivalent zinku rozpuštěny jen 2/3 ekvivalentu zlata v kyselině solné. To může vypadat podivně jen tehdy, když se jako Wiedemann držíme starých ekvivalentních vah a chlorid zinečnatý píšeme jako ZnCl, kde jak chlor, tak i zinek se objevují v chloridu jen s jednou valenční jednotkou. Ve skutečnosti v něm vězí na jeden atom zinku dva atomy chloru, ZnCl2 a jakmile tento vzorec známe, vidíme ihned, že v hořejším určováni ekvivalence je třeba vzít za jednotku atom chloru, a nikoli atom zinku. Vzorec pro chlorid zlatitý je však AuCl3 a podle toho je hned jasné, že 3ZnCl2 obsahují právě tolik chloru jako 2AuCl3 a že tedy ve všech primárních, sekundárních a terciárních procesech v článku nebo v elektrolytické lázni nutně bude reagovat na jeden váhový díl zinku přeměněný v chlorid zinečnatý ne méně a ne více než 2/3 váhového dílu[38] zlata v chloridu zlatitém. To platí absolutně, ledaže by sloučeninu AuCl3 bylo lze získat také elektrochemickou cestou; v tomto případě by byly na jeden ekvivalent zinku rozpuštěny dokonce dva ekvivalenty zlata, takže by tam pak - podle síly proudu - mohly nastat podobné variace jako u chloru a mědi. Význam Renaultových pokusů spočívá v tom, že ukazují, jak je Faradayův zákon potvrzován skutečnostmi, které mu zdánlivě odporují. Není však jasné, co měly přinést k osvětlení sekundárních procesů při elektrolyse.
Třetí příklad Wiedemannův vedl nás opět přímo od elektrolytické lázně k článku. A opravdu, článek má daleko největší zajímavost, pokud zkoumáme elektrolytické procesy s hlediska proměn energie, které přitom probíhají. Narazíme nezřídka na články, ve kterých jsou chemicko-elektrické procesy zdánlivě v přímém rozporu se zákonem o zachování energie a probíhají zdánlivě proti zákonům chemické afinity.
Podle Poggendorffových měření dává článek: zinek, koncentrovaný roztok NaCl, platina, proud o síle 134,6. Máme zde tedy zcela úctyhodné množství elektřiny, o jednu třetinu více než v Daniellově článku. Odkud pochází energie objevující se zde jako elektřina? „Primárním” pochodem je vytěsnění sodíku zinkem ze sloučeniny s chlorem. Ale v běžné chemii vytěsňuje nikoli zinek sodík, nýbrž naopak sodík vytěsňuje zinek z chlorových a jiných sloučenin. „Primární” pochod nejenže nemůže dodat proudu hořejší množství energie, naopak, sám potřebuje přívod energie zvenčí, aby mohl vůbec existovat. S pouhým „primárním” procesem se tedy zase nehneme s místa. Poohlédněme se tedy po skutečném pochodu. Pak zjistíme, že proměna není
Zn + 2NaCl = ZnCl2 + 2Na,
nýbrž
Zn + 2NaCl + 2H2O = ZnCl2 + 2NaOH + H2
Jinými slovy, sodík není volně vylučován na záporné elektrodě, nýbrž převáděn na louh jako v příkladě I (str. [123-124]).
Abychom vypočítali příslušné změny energie, k tomu nacházíme některé opěrné body v údajích Julia Thomsena. Podle něho je uvolněná energie při sloučeninách
(Zn, Cl2) =97.210
(ZnCl2, aqua) = 15.630,
celkem pro rozpuštěný chlorid zinečnatý 112.840 tepelných jedn.
(2Na, O, H, aqua) = 223.620 tepelných jed.
celkem 336.460 tepelných jedn.
Od toho odečteme spotřebu energie při rozkladech:
2(Na, Cl, aq) 193.020 tepelných jednotek
2(H2O) 136.720 tepelných jedn.
Celkem 329.740 tepelných jednotek.
Přebytek uvolněné energie tedy:
6720 tepelných jednotek.
Toto množství je zřejmě malé pro sílu proudu, požadovanou Poggendorffem, ale stačí, abychom vysvětlili jednak oddělení sodíku od chloru, jednak vznik proudu vůbec.
Zde máme pádný příklad, jak je rozlišování primárních a sekundárních pochodů zcela relativní a jak nás vede k absurdnostem, pokud je bereme absolutně. Primární elektrolytický proces, vzat sám o sobě, nejen nemůže vyrábět proud, ale nemůže ani sám proběhnout. Sekundární, zdánlivě čistě chemický proces je to právě, který primární pochod umožňuje a nadto dodává celý přebytek energie pro tvoření proudu. Ukázal se tedy ve skutečnosti procesem primárním a „primární” sekundárním. Když Hegel metafysikům a metafysicky myslícím přírodovědcům převracel jejich pevně navyklé rozdíly a protiklady dialekticky v opak, tikalo se, že překrucuje jejich slova. Jestliže se však příroda sama chová jako starý Hegel, pak je přece jen asi na čase, abychom věc blíže prozkoumali.
Větším právem můžeme za sekundární považovat ty procesy, které sice probíhají následkem chemicko-elektrického procesu v článku, nebo následkem elektro-chemického procesu v elektrolytické lázni, ale odděleně a nezávisle na něm, které tedy nastávají v určité vzdálenosti od elektrod. Proměny energie, probíhající při takovýchto sekundárních pochodech, nevstupují tedy do elektro-chemického procesu, ani mu neodebírají, ani nepřidávají energie. Takové procesy se vyskytují v elektrolytické lázni velmi hojně; měli jsme nahoře u příkladu I. případ tvoření kyseliny sírové při elektrolyse síranu sodného, zde však mají malou zajímavost. Naproti tomu jejich objevení v článku je prakticky mnohem důležitější: Neboť ačkoli chemicko-elektrickému procesu neubírají ani nepřidávají energii, mění přece součet energie, kterou v článku vůbec můžeme disponovat, a ovlivňují jej tak nepřímo.
Sem náleží, kromě dodatečných chemických proměn obyčejných, ty zjevy, které nastanou, když jsou ionty na elektrodách vylučovány v jiném stavu, než je ten, v němž se obvykle vyskytuji volně, a jestliže pak do svého normálního stavu přicházejí, až když se částečně vzdálily od elektrod. Ionty mohou přitom zaujmout jinou hustotu nebo jiné skupenství. Mohou však zaznamenat i významné změny ve své molekulární konstituci, a tento případ je nejzajímavější. Ve všech těchto případech odpovídá sekundární chemické nebo fysikální změně iontů, probíhající v určité vzdálenosti od elektrod, analogická změna tepla. Většinou se teplo uvolňuje, v jednotlivých případech spotřebovává. Tato změna tepla se omezuje samozřejmě na místo, kde nastává. Kapalina v článku nebo elektrolytické lázni se otepluje nebo ochlazuje, ostatní okruh zůstává změnou nedotčen; proto se toto teplo nazývá lokální. O ekvivalenci tohoto positivního nebo negativního lokálního tepla vyrobeného v článku se musí zvětšit, respektive zmenšit uvolněná chemická energie, kterou můžeme disponovat pro proměnu v elektřinu. V článku s peroxydem vodíku a kyselinou solnou byly podle Favra 2/3 veškeré uvolněné energie spotřebovány jako lokální teplo; Grovův článek se naproti tomu po zapojení značně ochlazoval a přiváděl tedy proudovému okruhu absorpcí tepla ještě energii zvenčí. Vidíme tedy, že i tyto sekundární procesy působí zpětně na pochod primární. Můžeme se postavit k problému, jak chceme, rozlišování mezi primárními a sekundárními procesy zůstává pouze relativní a ve vzájemném působení se zpravidla opět ruší. Zapomeneme-li na to, posuzujeme-li takové relativní protiklady jako absolutní, zapadneme nakonec, jak jsme výše viděli, beznadějně do rozporů.
Při elektrolytickém vylučování plynů pokrývají se, jak známo, elektrody tenkou vrstvou plynu; síla proudu následkem toho poklesne, až jsou elektrody nasyceny plynem, načež se zeslabený proud opět ustálí. Favre a Silbermann dokázali, že se v takové elektrolytické lázni objevuje lokální teplo, které může pocházet jen z toho, že se plyny na elektrodách neuvolňuji ve stavu, v němž se obyčejně objevují, nýbrž že jsou do svého normálního stavu uvedeny teprve delším procesem, spojeným s vývojem tepla. Ale v jakém stavu jsou plyny na elektrodách vylučovány? Nemůžeme se o tom vyslovit opatrněji než Wiedemann. Nazývá tento stav „určitý”, „anotropní”, „aktivní”, u kyslíku konečně několikrát „ozonisovaný”. U vodíku se vyjadřuje ještě tajemněji. Příležitostně projevuje názor, že ozon a peroxyd vodíku jsou formami, v nich se realisuje tento „aktivní” stav. Přitom pronásleduje ozon našeho autora tak, že dokonce některé extrémně elektronegativní vlastnosti superoxydů vysvětluje tím, že „možná obsahují část kyslíku v ozonisovaném stavu”! (I, str. 57)[39]. Rozhodně se tvoří při rozkladu vody jak ozon, tak i peroxyd vodíku, ale jen v nepatrných množstvích. Schází jakýkoli důkaz pro předpoklad, že lokální teplo je v tomto případě podmíněno právě vznikem a pak rozkladem značnějších množství těchto obou hořejších sloučenin. Slučovací teplo ozonu (O3) z volných atomů kyslíku neznáme. Slučovací teplo peroxydu vodíku z H2O (kapalné) + O je podle Berthelota rovno = 21.480; vznik této sloučeniny ve větším množství by tedy vyžadoval silného přívodu energie (až 30 % energie nutné k oddělení H2 a O), který by přece musel být nápadný a dokazatelný. Konečně by nám ozon a peroxyd vodíku pomohly jen u kyslíku (nepřihlížíme-li k obráceným proudům, kdy by se nám oba plyny objevily na těehže elektrodách), ale nikoli u vodíku. A přece uniká také vodík v „aktivním” stavu, a to tak, že v kombinaci: roztok dusičnanu draselného mezi platinovými elektrodami, se slučuje vodík s dusíkem vylučovaným z kyseliny přímo na amoniak.
Všechny tyto těžkosti a nesrovnalosti ve skutečnosti neexistují. Vylučování látek v „aktivním stavu” není monopolem elektrolytického procesu. Každý chemický rozklad dokáže totéž. Vylučuje chemické prvky nejprve ve formě volných atomů O, H, N atd., které se teprve po svém uvolnění mohou spojovat do molekul O2, H2, N2 atd. a při tomto spojení vydávají jisté, dnes ještě nezjistitelné množství energie, které se projeví jako teplo. Během mizivě nepatrného okamžiku, kdy jsou tyto atomy volné, jsou nositeli celého množství energie, kterou vůbec mohou na sebe vzít; mají-li maximum své energie, mohou vejít v jakoukoli kombinaci, která se jim naskýtá. Jsou tedy „v aktivním stavu” proti molekulám O2, H2, N2, které už jistou část své energie odevzdaly a nemohou se sloučit s jinými prvky, pokud jim nebude tato odevzdaná energie zvenčí přivedena zpět. Nemáme tedy naprosto zapotřebí nejprve se utíkat k ozonu a peroxydu vodíku, které jsou teprve produkty onoho aktivního stavu. Můžeme na př. zmíněné tvoření amoniaku při elektrolyse dusičnanu draselného uskutečnit také jednoduše bez článku chemicky, když přidáme kyselinu dusičnou a roztok dusičnanu k nějaké kapalině, v níž se chemickým procesem uvolňuje vodík. Aktivní stav vodíku je v obou případech stejný. Nejzajímavější však na elektrolytickém procesu je to, že pomíjivá existence volných atomů je zde takřka hmatatelná. Pochod se dělí na dvě fáze: elektrolysa dodává volné atomy na elektrodách, ale jejich sloučení v molekuly nastává teprve v jisté vzdálenosti od elektrod. Ačkoli je tato vzdálenost mizivě malá vůči poměrům mezi masami, stačí, aby znemožnila, alespoň z největší části, vydání energie uvolněné při tvorbě molekul na elektrický proces, a tím způsobila proměnu této energie v teplo, a to v lokální teplo v článku. Tím je však zjištěno, že prvky byly vyloučeny jako volné atomy a že nějaký čas v článku jako volné atomy existovaly. Tato skutečnost, kterou můžeme v čisté chemii zjistit jen theoretickými závěry, je nám zde experimentálně dokázána, pokud je to možné bez smyslového vnímání atomů a molekul samých. A v tom spočívá ohromný vědecký význam t. zv. lokálního tepla článku.
Proměna chemické energie v elektřinu přes článek je pochod, o jehož průběhu nevíme skoro nic a také se asi nic bližšího nedovíme, dokud nebude lépe znám modus operandi elektrického pohybu samého.
Článku se připisuje určitá „elektrická rozdělovací síla”, která je pro určitý článek vždy stejná. Jak jsme viděli hned na začátku, Wiedemann přiznává, že tato elektrická rozdělovací síla není jen nějaká určitá forma energie. Naopak, je to jen schopnost, vlastnost článku proměnit v časové jednotce určité množství uvolněné chemické energie v elektřinu. Tato chemická energie nedostává v celém průběhu procesu formu t. zv. „elektrické rozdělovací síly”, nýbrž naopak, dostává hned a bezprostředně formu . t. zv. „elektromotorické síly”, t. j. elektrického pohybu. Mluví-li se v obyčejném životě o síle nějakého parního stroje v tom smyslu, že je schopen v jednotce časové proměnit určité množství tepla v pohyb hmoty, není v tom žádný důvod, abychom tento zmatek zaváděli také do vědy. Právě tak by se mohlo mluvit o rozličné síle pistole, karabiny, pušky s hladkou hlavní nebo s drážkovanou, protože při stejné náloži prachu a stejné váze náboje mají různý dostřel. Zde je nesmyslnost takového vyjadřování zřejmá. Každý ví, že je to roznícení prachové náplně, která pohání střelu, a že různý dostřel zbraně je podmíněn větším nebo menším vydáním energie, podle délky hlavně, přesnosti ráže střely[40] a jejího tvaru. Stejný případ. je však síla páry a elektrická rozdělovací síla. Dva parní stroje při jinak stejných podmínkách, t. j. že za stejnou dobu se uvolňují stejná množství energie, nebo dva galvanické články, o nichž platí totéž, se rozlišují ve svých výkonech větším nebo menším mrháním energií. A jestliže se dosud technika palných zbraní všech armád obešla bez nějaké zvláštní předpokládané „střelné” síly pušek, nemá věda o elektřině žádnou výmluvu pro před. poklad nějaké „elektrické rozdělovací síly”, analogické střelné síle, síly, v níž nevězí naprosto žádná energie a která tedy sama ze sebe nemůže vykonat ani miliontinu miligrammilimetru práce.
Totéž platí o druhé formě této „rozdělovací síly”, o „elektrické kontaktní síle kovu”, o níž se zmiňuje Helmholtz. Není to nic jiného než vlastnost kovu měnit kontaktem existující energii jiné formy na elektřinu. Je tedy rovněž silou, která nemá ani jiskřičku energie. Předpokládejme s Wiedemannem, že zdroj energie kontaktní elektřiny je v živé síle adhesních pohybů. Pak existuje tato energie nejprve ve formě tohoto pohybu hmot a proměňuje se při svém zmizení hned v elektrický pohyb, aniž, byť i na okamžik, přijímá formu „elektrické kontaktní síly”.
A k tomu se nám nyní ještě tvrdí, že tato „elektrická rozdělovací síla”, která nejen žádnou energii neobsahuje, ale ani podle svého pojetí obsahovat nemůže, je úměrná elektromotorické síle, t. j. chemické energii, objevující se opět jako elektrický pohyb! Tato úměrnost mezi neenergií a energií patří zřejmě do téže kategorie matematiky, ve které figuruje „poměr mezi jednotkou elektřiny a miligramem”. Za absurdní formou, která děkuje za svůj vznik chápání prosté vlastnosti jako nějaké mystické síly, vězí však pouhá, zcela jednoduchá tautologie: schopnost určitého článku měnit uvolněnou chemickou energii v elektřinu se měří - čím? Prostě poměrem množství energie, objevující se znovu ve vodivém okruhu jako elektřina, k chemické energii spotřebované v článku. To je vše.
Abychom se však dostali k elektrické rozdělovací síle, musíme brát vážně pomocný pojem dvou elektrických fluid. Abychom je z jejich neutrality převedli do jejich polarity, abychom je tedy od sebe odtrhli, k tomu je ,potřebí vynaložit určitou energii elektrickou rozdělovací sílu. Jestliže jsou tyto elektřiny již jednou od sebe odtrženy, mohou při svém opětném spojení opět odevzdat totéž množství energie ― elektromotorickou sílu. Ale protože dnes žádný člověk, ani sám Wiedemann, nepovažuje tyto dvě elektřiny za skutečně existující, pak, kdybychom se do podobného uvažování chtěli pustit hlouběji, znamenalo by to psát pro dávno zesnulé publikum.
Základní omyl kontaktní theorie spočívá tedy v tom, že se nemůže odtrhnout od představy, že kontaktní síla nebo elektrická rozdělovací síla je nějakým zdrojem energie. Zbavit se této představy bylo ovšem těžké, když byla prostá vlastnost aparátu - zprostředkování proměny energie - proměněna v sílu; neboť síla má být právě určitou formou energie. Protože se Wiedemann nemůže zbavit této nejasné představy síly, ačkoli se mu vedle ní vnucují moderní představy o nezničitelné a nestvořitelné energii, upadá v ono nesmyslné vysvětlování proudu čís. 1 a ve všechny ty později dokázané rozpory.
Je-li výraz „elektrická rozdělovací síla” přímo protismyslný, je druhý - „elektromotorická síla” - při nejmenším zbytečný. Měli jsme tepelné stroje dříve, než jsme měli elektromotory, a přece se theorie tepla obešla docela dobře bez nějaké zvláštní thermomotorické síly. Jako jednoduchý výraz „teplo” v sobě shrnuje všechny ty pohybové jevy, které náležejí k této formě energie, právě tak je může zahrnout výraz „elektřina” ve svém oboru. Přitom nejsou mnohé formy působení elektřiny vůbec přímo „motorické”: magnetisování železa, chemický rozklad, proměna v teplo. A konečně je v každé přírodní vědě, i v mechanice pokrokem, když se nějakým způsobem vypořádáme se slovem síla.
Viděli jsme, že Wiedemann přijal chemický výklad pochodů v článku do jisté míry neochotně. Tato neochota ho provází neustále; kde může t. zv. chemické theorii něco vytknout, jistě tak učiní. Tak na příklad poznamenává, že „není naprosto dokázáno, že elektromotorická síla je úměrná intensitě chemického působení” (I., str. 791). Ovšemže v každém případě není. Kde však tato úměrnost nenastává, je to jen důkaz pro to, že článek je špatně konstruován, že v něm nastávají ztráty energie. A proto má Wiedemann zcela pravdu, když ve svých theoretických vývodech nebere žádný ohled na takové vedlejší okolnosti, které čistotu procesu jen kazí, a stručně zjišťuje, že elektromotorická síla článku se rovná mechanickému ekvivalentu chemického působení, probíhajícího v článku za jednotku času při jednotce intensity proudu.
Na jiném místě čteme: ,,Že dále v kyselo-alkalickém článku není spojení kyseliny a louhu příčinou vzniku proudu, plyne z pokusů § 61 (Becquerel a Fechner) , § 260 (Dubois-Reymond), § 261 (Worm-Müller), podle nichž v určitých případech, když jsou kyselina a louh v ekvivalentním množství, nevzniká žádný proud; rovněž to plyne z pokusu uvedeného v § 62 (Henrici) , podle něhož elektromotorická síla po vpojení roztoku dusičnanu draselného mezi draselný louh a kyselinu dusičnou vzniká stejně jako před zapojením” (I, str. 791)[41].
Otázka, zda slučování kyseliny a louhu je příčinou vzniku proudu, zaměstnává našeho autora velmi vážně. Je na ni možno v této formě snadno odpovědět. Spojení kyseliny a louhu je především příčinou vzniku soli při současném uvolnění energie. Zda tato energie nabude úplně nebo zčásti formy elektřiny, závisí na okolnostech, za nichž je uvolňována. Na př. v článku: kyselina dusičná a louh draselný mezi platinovými elektrodami ― stane se to při nejmenším částečně, při čemž je pro vytvoření proudu lhostejné, zda mezi kyselinu a louh vložíme dusičnan čili nic, neboť to může vznik proudu nanejvýš zpomalit, ale nikoli mu zabránil. Vezmeme-li však článek, jako je Worm Müllerův, na nějž se Wiedemann stále odvolává, kde jsou kyselina a louh uprostřed a roztok jejich solí na obou koncích - a to ve stejné koncentrací jako roztok tvořící se v článku - pak nemůže samozřejmě vzniknout žádný proud, neboť vlivem koncových členů - protože se všude tvoří identické látky - nemohou vzniknout žádné ionty. Bylo zde tedy proměně uvolněné energie v elektřinu zabráněno tak přímo, jako bychom vůbec nezapjali okruh; nemůžeme se tedy divit, když nedostaneme proud. Že však kyselina a louh vůbec proud vyrobit mohou, dokazuje článek: uhlík, kyselina sírová (1 díl na 10 dílů vody), louh draselný (1 díl na 20 dílů vody), uhlík, - článek, který má podle Raoulta sílu proudu 73[*29]; a že kyselina a louh mohou při vhodném uspořádání článku vydat sílu proudu odpovídající velké uvolněné energii, vyplývá z toho, že nejsilnější známé články spočívají skoro výhradně na tvorbě zásaditých solí, na př. u Wheatstona: platina, chlorid platinčitý, draselný amalgam, síla proudu - 230; peroxyd olova, zředěná kyselina sírová, amalgam draslíku - 326; peroxyd manganu místo peroxydu olova - 280; přitom když bylo místo amalgamu draslíku použito amalgamu zinkového, klesla síla proudu po každé skoro přesně o 100. Podobně obdržel Beetz v článku: pevný kalomel, roztok manganistanu draselného, louh draselný, draslík - sílu proudu 302; dále: platina, zředěná kyselina sírová, draslík 293,8; Joule: platina, kyselina dusičná, louh draselný, draselný amalgam - 302. „Příčinou” těchto výjimečně silných proudů je ovšem spojení kyseliny s louhem, resp. alkalickým kovem a velké množství energie, přitom uvolněné.
O několik stránek dále čteme opět: „Je nutno si pečlivě povšimnout, že za míru elektromotorické síly v článku nelze považovat přímo pracovní ekvivalent celého chemického působení heterogenních těles, objevujícího se na kontaktním místě. Když na př. v Becquerelově kyselino-louhovém článku (iterum Crispinus!)[42] se slučují obě tyto látky; když v článku: platina, roztavený dusičnan sodný, uhlík - se uhlík spaluje; když v obyčejném článku: měď, nečistý zinek, zředěná kyselina sírová - se zinek za tvoření lokálních proudů rychle rozpouští, pak je veliká část práce, provedené při těchto chemických procesech (mělo by znít: uvolněné energie...), proměňována v teplo a je tak pro celý okruh ztracena” (I, str. 798). Všechny tyto procesy lze převést na ztrátu energie v článku. Nedotýkají se skutečnosti, že elektrický pohyb vzniká z přeměněné chemické energie, dotýkají se jenom množství této energie.
Badatelé v oboru elektřiny věnovali nekonečný čas a námahu na sestavení nejrůznějších článků a na měření jejich „elektromotorické síly”. Nahromaděný tak materiál obsahuje mnoho cenného, ale ještě mnohem více bezcenného. Jaký vědecký význam mají na př. pokusy, při nichž se jako elektrolytu používá „vody”, která, jak nyní dokázal F. Kohlrausch, je nejhorším vodičem, a tedy také nejhorším elektrolytem, kde tedy nezpůsobuje procesy voda, nýbrž neznámé znečistěniny?[*30] A přece spočívá na př. skoro polovina všech pokusů Fechnerových na takovémto použití vody, dokonce i jeho „experimentum crucis”,[43] kterým chtěl na troskách chemické theorie vytvořit neotřesitelnou theorii kontaktní. Jak již z toho vyplývá, jsou vůbec skoro ve všech pokusech, vyjma několik málo, téměř úplně ignorovány chemické pochody v článku, které jsou pravým zdrojem t. zv. elektromotorické síly. Existuje však celá řada článků, z jejichž chemické formulace nemůže být učiněn žádný spolehlivý závěr na chemické procesy, probíhající v nich po zapnutí proudu. Naopak, jak říká sám Wiedemann, (I., str. 797), „nelze popřít, že v článku nemůžeme ještě ani zdaleka ve všech případech porozumět všem chemickým afinitám”. Všechny tyto experimenty jsou tedy vzhledem k stále důležitější chemické stránce potud bezcenné, pokud nebudou opakovány za kontroly chemických pochodů.
O proměnách energie, probíhajících v článku, se v těchto pokusech mluví jen výjimečně. Mnohé byly provedeny dříve, než byl přírodovědecky uznán zákon ekvivalence pohybu, jsou však vlečeny ze zvyklosti z jedné příručky do druhé, nepřezkoumány a neuzavřeny. Jestliže se dříve říkalo, že elektřina nemá setrvačnost (což má asi tolik smyslu, jako kdyby se řeklo, že rychlost nemá specifickou váhu), pak se to nikterak nemůže tvrdit o nauce o elektřině.
Posuzovali jsme dosud galvanický článek jako zařízení, v němž se následkem kontaktních podmínek nějakým ― až dosud neznámým ― způsobem uvolňuje chemická energie a proměňuje v elektřinu. Stejně jsme mluvili o elektrolytické lázni jako o zařízení, v němž probíhá opačný pochod: elektrolytický pohyb se proměňuje v chemickou energii a je jako takový spotřebován. Musili jsme přitom do popředí stavět chemickou stránku procesu, tak zanedbávanou badateli v oboru elektřiny, protože to byla jediná cesta, jak se zbavit chaosu představ, převzatých ze staré kontaktní theorie a z učení o dvou elektrických fluidech. Jakmile se tak stalo, jde ještě o to, zda chemický pochod v článku probíhá za těchže podmínek jako mimo něj, nebo zda se přitom vyskytují zvláštní zjevy, závislé na elektrickém napětí.
Nesprávné představy jsou konec konců, nehledíme-li k omylům při pozorování, v každé vědě nesprávnými představami o správných skutečnostech. Skutečnosti zůstávají, i když byly představy odhaleny jako chybné. Když jsme setřásli starou kontaktní theorii, zůstávají ještě zjištěné okolnosti, k jejichž vysvětlení sloužila. Všimněme si jich a zároveň i vlastní elektrické stránky pochodu v článku.
Není sporu o tom, že při kontaktu heterogenních těles při současných chemických změnách nebo i bez nich je vzbuzena elektřina, kterou lze prokázat elektroskopem nebo galvanometrem. Zdroj těchto nanejvýš minimálních pohybových jevů je v jednotlivém případě, jak jsme viděli již z počátku, těžko zjistitelný; stačí, připouštíme-li obecně existenci takovéhoto vnějšího zdroje.
Kohlrausch uveřejnil v letech 1850-1853 serii pokusů, v nichž po dvou sestavil jednotlivé součásti článku a zkoumal statickoelektrická napětí, vždy prokazatelná. Z algebraického součtu těchto napětí se má pak skládat elektromotorická síla článku. Tak vypočetl, bereme-li napětí Zn/Cu = 100, relativní elektromotorickou sílu Daniellova a Grovova článku:
Daniell:
Zn/Cu + amalg. Zn/H2SO4 + Cu/SO4Cu =
100 + 149 – 21 = 228,
Grove:
Zn/Pt + amalg. Zn/H2SO4 + Pt/HNO3 =
107 + 149 + 149 = 405,
což skoro souhlasí s přímým měřením síly proudu těchto článků. Tyto výsledky však naprosto nejsou spolehlivé. Především Wiedemann sám upozorňuje na to, že Kohlrausch uveřejňuje jen konečný výsledek, ale „bohužel, žádné číselné údaje o výsledcích jednotlivých pokusů”.[44] A za druhé, Wiedemann sám uznává, že všechny pokusy určit kvantitativně elektrická napětí při kontaktu kovů, a ještě více při kontaktu kovu a kapaliny, jsou pro mnohé nevyhnutelné zdroje chyb při nejmenším velmi nespolehlivé. Jestliže přesto s Kohlrauschovými čísly počítá, učiníme lépe, nebudeme-li ho v tom následovat, tím spíše, že existuje jiný určovací prostředek, proti kterému nemohou být vznášeny takové námitky.
Ponoříme-li dvě elektrody článku do kapaliny a spojíme-li je pak s konci galvanometru do vodivého okruhu, je podle Wiedemanna „počáteční výchylka magnetky galvanometru, dříve než chemické změny mohou pozměnit sílu vzbuzené elektřiny, mírou pro součet elektromotorických sil v okruhu”[45]. Různě silné články dávají tedy různě velké počáteční výchylky a velikost těchto výchylek je úměrná síle proudu příslušného článku.
To by vypadalo tak, jako bychom zde měli před sebou „elektrickou rozdělovací sílu”, „kontaktní sílu”, působící pohyb nezávisle na jakémkoli chemickém působení. Tak se skutečně domnívá celá kontaktní theorie. A skutečně, zde máme vztah mezi elektřinou a chemickým působením, který jsme dosud nezkoumali. Abychom se k němu dostali, všimněme si nejprve trochu blíže t. zv. elektromotorického zákona; uvidíme přitom, že také zde tradiční kontaktní představy nejen nepodávají vysvětlení, nýbrž dokonce cestu k němu přímo uzavírají.
Jestliže do libovolného článku z dvou kovů a kapaliny, na př. zinku, zředěné kyseliny solné a mědi, vložíme nějaký třetí kov, na př. platinovou destičku, aniž ji spojíme vodivým drátem s vnějším vodivým okruhem, je původní výchylka galvanometru právě taková jako bez platinové destičky. Ta tedy nepůsobí na vznik elektřiny. Tak jednoduše se to však v elektromotorické řeči nemůže vyjádřit. Zde to zní takto:
„Na místo elektromotorické síly zinku a mědi v kapalině nastoupil teď součet elektromotorických sil zinku a platiny a platiny a mědi. Protože cesta elektřiny není vložením platiny znatelně pozměněna, můžeme z rovnosti údajů galvanometru v obou případech usuzovat, že elektromotorická síla zinku a mědi v kapalině je rovna elektromotorické síle zinku a platiny plus elektromotorická síla platiny a mědi v téže kapalině. To by odpovídalo theorii vytvořené Voltou pro vznik elektřiny mezi samotnými kovy. Výsledek, který platí pro všechny libovolné kapaliny a kovy, vyslovuje se takto:
Kovy se řídí při vzniku elektromotorické síly v kapalinách zákonem Voltovy řady. Označujeme tento zákon také jménem elektromotorického zákona”. (Wiedemann, I, str. 62.)
Řekneme-li, že platina nepůsobí při této kombinaci vůbec na vznik proudu, vyslovíme tím prostý fakt. Řekneme-li, že sice působí elektricky, ale ve dvou opačných směrech se stejnou silou, takže účinek se ruší, pak se fakt promění v hypothesu, prostě jen abychom vzdali čest „elektromotorické síle”. V obou případech hraje platina úlohu bezvýznamného statisty.
Při prvním výkyvu neexistuje ještě žádný vodivý okruh. Pokud se kyselina nezačala rozkládat, nevede proud, činí tak jen pomocí iontů. Jestliže tedy třetí kov nepůsobí na původní výchylku, pak to prostě pochází z toho, že je ještě isolován.
Jak se chová třetí kov po zavedení trvalého proudu a za jeho trvání?
Voltova řada kovů ve většině kapalin má zinek vzhledem k alkalickým kovům značně na positivní straně a platinu na straně negativní. Měď stojí uprostřed. Je-li tedy platina, jako nahoře, postavena mezi měď a zinek, je vůči oběma negativní; proud v kapalině, pokud by platina vůbec působila, by musil téci od zinku a od mědi k platině, tedy od obou elektrod k nezapojené platině; což je contradictio in adjecto.[46] Základní podmínka působnosti více kovů v článku je právě v tom, že jsou zvenčí napojeny na vodivý okruh. Nespojený, přespočetný třetí kov v článku funguje jako nevodič; nemůže tedy ani ionty vytvářet, ani je propouštět, a bez iontů nemáme v elektrolytech žádné vedení proudu. Je tedy tento třetí kov nejen statistou, stojí dokonce iontům v cestě a nutí je prodírat se stranou vedle něho.
Podobně je tomu, spojíme-li zinek s platinou a necháme měď nezapojenou uprostřed: zde by měď, kdyby vůbec působila, vytvářela proudy od zinku k mědi a od mědi k platině, sloužila by tedy jako jakási mezielektroda. Na straně přivrácené. k zinku by se vylučoval plynný vodík, což je opět nemožné.
Setřeseme-li se sebe tradiční elektromotorický způsob vyjadřování, jeví se nám případ velmi jednoduše. Galvanický článek je, jak jsme viděli, zařízení, v němž se uvolňuje chemická energie a proměňuje v elektřinu. Skládá se zpravidla z jedné nebo více kapalin a dvou kovů jako elektrod, které musí být mimo kapalinu mezi sebou vodivě spojeny. Tím je aparát sestaven. Co ještě do elektrolytu nezapojeno přidáme dále, ať je to kov, sklo, pryskyřice nebo cokoli jiného, nemůže se zúčastnit chemicko-elektrického procesu probíhajícího v článku, t. j, tvoření proudu, pokud nemění chemicky kapalinu; může proces nanejvýš rušit. Ať je elektromotorická schopnost třetího vnořeného kovu vůči kapalině nebo jedné či oběma elektrodám čímkoli, nemůže působit, pokud třetí kov není mimo kapalinu spojen do vodivého okruhu.
Podle toho je tedy chybné nejen hořejší Wiedemannovo odvození t. zv. elektromotorického zákona; také smysl, který tomuto zákonu dává, je chybný. Nemůžeme mluvit ani o navzájem se kompensujících elektromotorických účincích nezapojeného kovu, poněvadž tomuto kovu byla odňata jediná podmínka, za níž může působit; ani nemůže být t. zv. elektromotorický zákon odvozen ze skutečnosti, která je mimo sféru jeho kompetence.
Starý Poggendorff uveřejnil roku 1854 serii pokusů, při nichž měřil elektromotorickou sílu nejrůznějších článků, t. j. množství elektřiny, dodávané jimi za jednotku časovou. Z nich má zvláštní cenu prvních 27 pokusů, ve kterých spolu spojil v témže elektrolytu tři určité kovy do tří rozdílných článků a zkoumal dodávané množství elektřiny a pak je vzájemně porovnával. Jako zarytý přívrženec kontaktní theorie ponechal v článku vždy i třetí nezapojený kov a měl tak zadostiučinění se přesvědčit, že ve všech 81 článcích zůstal tento „třetí v spolku”[47] v roli bezvýznamného statisty. V tom však význam těchto pokusů nikterak nespočívá, nýbrž je v potvrzení a zjištění správného smyslu t. zv. elektromotorického zákona.
Zůstaňme u hořejší tady článků, kde jsou do zředěné kyseliny solné ponořeny zinek, měď a platina a vždy po dvou spojeny. Zde nalezl Poggendorff tato dodaná množství elektřiny (Daniellův článek 100):
zinek - měď 78,8
měď - platina 74,3
dohromady 153,1
zinek - platina 153,7[48]
Zinek v přímém spojení s platinou dává tedy skoro totéž množství elektřiny jako zinek s mědí plus měď s platinou. Totéž nastalo i u všech ostatních článků, ať bylo použito jakýchkoli kapalin a kovů. Byly-li z řady kovů vytvořeny články tak, že v témže elektrolytu (podle Voltovy řady kovů, platné pro tuto kapalinu) bylo druhého, třetího, čtvrtého atd. kovu použito jako negativní elektrody pro předcházející a jako kladné elektrody pro následující kov, je součet všech množství elektřiny, dodaných těmito články, roven množství elektřiny, dodanému článkem přímo mezi oběma koncovými kovy celé řady. Bylo tedy na př. množství elektřiny dodané ve zředěné kyselině solné články: zinek-cín, cín-železo, železo-měď, měď-stříbro, stříbro-platina dohromady rovné množství elektřiny dodanému článkem zinek-platina; baterie, sestavená z těchto článků, by se právě neutralisovala, za jinak stejných podmínek, článkem zinek-platina, zapojeným v obráceném smyslu.
V tomto pojetí má t. zv. elektromotorický zákon skutečný a značný význam. Odbaluje novou stránku vztahu mezi chemickým a elektrickým působením. Až dosud, při zkoumání hlavně zdroje energie galvanického proudu, se jevil tento zdroj, chemická proměna, aktivní stránkou procesu; elektřina byla jím vyráběna, jevila se tedy pasivní. Nyní se to obrací. Elektrické napětí, způsobené složením heterogenních těles, přicházejících v článku do kontaktu, nemůže chemickému působení energii ani dodávat, ani ubírat (jinak než přeměnou uvolňující se energie v elektřinu). Ale může, podle zařízení článku, tuto akci zrychlit nebo zpomalit. Jestliže článek zinek-zředěná kyselina solná-měď dává za jednotku času jen polovinu oné elektřiny, kterou dodává článek zinek-zředěná kyselina solná-platina, pak to znamená, chemicky vyjádřeno, že první článek tvoří v jednotce času jenom poloviční množství chloridu zinečnatého a vodíku oproti druhému článku. Chemická akce se tedy zdvojnásobila, ačkoli její čistě chemické podmínky zůstaly nezměněny. Vznikající elektřina se tedy stává regulátorem chemického působení: je nyní aktivní stránkou celého procesu, chemické působení stránkou pasivní.
Pak je ovšem pochopitelné, že celá řada procesů, dříve považovaných za čistě chemické, jeví se nyní jako elektrochemické. Na chemicky čistý zinek působí zředěná kyselina jen nepatrně, pokud vůbec na něj působí; obyčejný, technický zinek se naproti tomu rozpouští rychle za současného tvoření soli a vyvíjení vodíku. Obsahuje příměsi jiných kovů a uhlíku, které jsou na různých místech jeho povrchu nestejně silně zastoupeny. Mezi nimi a zinkem samým se tvoří lokální proudy, při čemž zinková místa jsou positivní, ostatní kovy negativní elektrodou; na nich se vylučují bublinky vodíku. Podobně je nyní zjev, že železo ponořené do roztoku modré skalice se pokrývá vrstvičkou mědi, považován za elektrochemický, t. j. podmíněný proudy, které vznikají mezi heterogenními místy povrchu železa.
Podle toho také zjistíme, že Voltovy řady v kapalinách vcelku odpovídají pořadí, v kterém jsou kovy navzájem vytěsňovány ze svých sloučenin s halogeny a radikály kyselin. Na nejzazším negativním konci nalézáme zpravidla kovy skupiny zlata: zlato, platina, paladium, rhodium, které jsou těžko oxydovatelné, na které kyseliny nepůsobí skoro vůbec nebo jen nepatrně a které jsou ze svých solí lehce vytěsňovány jinými kovy. Na nejzazším positivním konci stojí alkalické kovy, které jeví chování právě opačné: jsou ze svých oxydů vylučovány teprve po vynaložení velké energie, nacházejí se v přírodě skoro výhradně ve formě solí a mají ze všech kovů daleko největší afinitu k halogenům a radikálům kyselin. Mezi nimi stojí ostatní kovy v trochu se měnícím pořadí, ale přece tak, že se jejich chemické a elektrické chování vcelku shoduje. Pořadí jednotlivých kovů se mění podle kapalin a je sotva pro některý elektrolyt definitivně stanoveno. Je dokonce možno pochybovat, zda pro určitou kapalinu existuje taková absolutní Voltova řada. Dva kusy téhož kovu mohou ve vhodných článcích a elektrolytických lázních působit jako positivní, nebo jako negativní elektroda. Tentýž kov tedy může být vůči sobě jak positivní, tak negativní. V thermočláncích, které proměňují teplo v elektřinu, nastává při vysokých rozdílech teploty na obou spájených místech změna směru proudu na opačný; dříve positivní kov se stává negativní a naopak. Právě tak neexistuje absolutní řada, ,podle níž by byly kovy vytěsňovány ze svých chemických sloučenin s určitým halogenem nebo radikálem kyseliny; přivedením energie ve formě tepla můžeme řadu platící pro normální teplotu v mnoha případech skoro libovolně pozměňovat a obracet.
Nalézáme zde tedy zvláštní vzájemné působení mezi chemismem a elektřinou. Chemická akce v článku, která dodává celou energii pro tvoření proudu, je sama v mnoha.případech uvedena v chod teprve elektrickými napětími, vytvořenými v článku, a ve všech případech je jimi kvantitativně regulována. Jestliže se nám dříve pochody v článku jevily jako chemicko-elektrické, vidíme zde nyní, že jsou právě tak elektrochemické. Se stanoviska tvoření trvalého proudu je chemické působení primární, se stanoviska vzbuzení proudu je sekundární, následné. Vzájemné působení vylučuje vše absolutně primární a absolutně sekundární; ale právě tak je to dvojstranný proces, který může být podle své povahy posuzován se dvou rozdílných stanovisek; aby mu bylo porozuměno jako celku, musí být zkoumán postupně s obou rozdílných stanovisek, dříve než může být shrnut celkový závěr. Držíme-li se však jednoho stanoviska jako absolutního oproti druhému, nebo přeskakujeme-li libovolně od jednoho k druhému jen podle okamžité potřeby argumentace, uvázneme v jednostrannosti metafysického myšlení; souvislost nám uniká a zamotáváme se do jednoho rozporu za druhým.
Viděli jsme už dříve, že podle Wiedemanna původní výchylka galvanometru, bezprostředně po ponoření kovových destiček do kapaliny a dříve než chemické účinky změnily sílu elektrického napětí, „je mírou pro součet elektromotorických sil ve vodivém okruhu”.
Až dosud jsme poznali t. zv. elektromotorickou sílu jako formu energie, která byla v našem případě získávána v ekvivalentním množství z chemické energie a která se v dalším průběhu proměňovala opět v ekvivalentní množství tepla, pohybu hmot atd. Zde se najednou dovídáme, že „součet elektromotorických sil v okruhu” existuje, dříve než chemické změny onu energii uvolní; jinými slovy, že elektromotorická síla článku není nic jiného než kapacita určitého článku, schopnost uvolnit v jednotce času určitou kvantitu chemické energie a proměnit ji v elektrický pohyb. Jako dříve elektrická rozdělovací síla, tak se nám zde jeví i elektromotorická síla jako síla, která nemá ani jiskřičku energie. Wiedemann tedy rozumí pod „elektromotorickou silou” dvě zcela rozdílné věci: jednak - schopnost určitého článku uvolnit určité množství chemické energie a proměnit je v elektrický pohyb, jednak - vyvinutý elektrický pohyb sám. Že jsou obě dvě navzájem úměrné, že jsou jedna mírou pro druhou, to neruší jejich rozdílnost. Chemické působení v článku, množství vyvinuté elektřiny a teplo, vzniklé z ní v okruhu (není-li mimo to vykonána žádná práce), jsou více než úměrné, jsou dokonce ekvivalentní; to však není nikterak na závadu jejich různosti. Schopnost parního stroje určitého vrtání a zdvihu vyrobit určité množství mechanického pohybu z přivedeného tepla je velmi rozdílná od onoho mechanického pohybu samého, jakkoli je mu úměrná. A byl-li takový způsob vyjadřováni snesitelný svého času, kdy se v přírodovědě ještě nemluvilo o zachování energie, přece jen je jasné, že od doby uznání tohoto základního zákona nesmí být skutečná živá energie v jakékoli formě zaměňována se schopností libovolného aparátu udělit uvolněné energii tuto formu. Tato záměna je doplňkem záměny síly a energie v případě elektrické rozdělovací síly; v obou se harmonicky spojují tři úplně si odporující vysvětlení proudu, a ty jsou základem všech Wiedemannových omylů a chyb s t. zv. „elektromotorickou silou”.
Kromě onoho právě uvedeného zvláštního vzájemného působeni mezi chemismem a elektřinou je ještě jedna spojitost, která rovněž dává tušit úzký vztah těchto dvou forem pohybu. Obě mohou existovat jen dočasně. Chemický proces probíhá pro každou skupinu atomů vstupující do něho okamžitě. Může být udržen jenom přítomností nového materiálu, nepřetržitě do něho vstupujícího. Podobně je tomu u elektrického pohybu. Sotvaže byl vyroben z nějaké jiné formy pohybu, už se opět obrací v třetí formu pohybu; jen neustálý přítok vhodné energie může vyrobit trvalý proud; v něm stále nová množství pohybu v každém okamžiku dostávají formu elektřiny a opět ji ztrácejí.
Pochopení tohoto úzkého vztahu mezi chemickým a elektrickým působením a naopak povede v obou oborech bádání k velkým výsledkům. Již teď se stále šiří. Mezi chemiky Lothar Mayer a po něm Kekulé přímo prohlásili, že před námi je opět elektrochemická theorie v omlazené formě. Také u badatelů v oboru elektřiny se zdá, jak naznačují zejména nejnovější práce F. Kohlrausche, že se konečně prosazuje přesvědčení, že jen přesné sledování chemických procesů v článku a v elektrolytické lázni může pomoci vědě ze slepé uličky starých tradic.
A vskutku, je možno považovat za nesporné, že nauka o galvanismu, a tím v druhé linii o magnetismu a statické elektřině může dostat pevnou základnu jen chemicko-exaktní generální revisí všech starých, tradičních, nekontrolovaných pokusů, stojících na překonaném vědeckém stanovisku, při současném přesném sledování proměn energie a předběžném odstranění všech tradičních theoretických představ o elektřině.